题目内容
【题目】有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6molL﹣1的H2SO4溶液中,乙同学将电极放入6molL﹣1的NaOH溶液中,如图所示.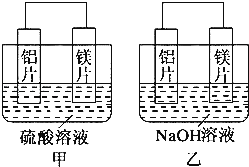
(1)甲中SO42﹣移向极(填“铝片”或“镁片”).写出甲中正极的电极反应式 .
(2)乙中负极为 , 总反应的离子方程式: . 此反应中氧化剂和还原剂的物质的量之比为 .
(3)上述实验也反过来证明了“直接利用金属活动性顺序表判断原电池中的正负极”这种做法(填“可靠”或“不可靠”).如不可靠,请你提出另一个判断原电池正负极的可行性实验方案(如可靠,此空可不填).
【答案】
(1)镁片;2H++2e﹣=H2↑
(2)铝片;2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑;3:1
(3)不可靠;在两电极之间连上一个电流计测电流方向,判断原电池的正负极
【解析】(1)镁易失电子作负极、Al作正极,负极上镁发生氧化反应、正极上氢离子发生还原反应,原电池中阴离子向负极移动,所以硫酸根离子流向镁片,正极的电极反应式为:2H++2e﹣=H2↑,所以答案是:镁片;2H++2e﹣=H2↑;(2)在碱性介质中铝比镁活泼,所以乙池中铝易失电子作负极、镁作正极,负极上铝失电子发生氧化反应,总的电极反应式为:2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑,氧化剂是水,还原剂是铝,而1mol的水电离产生1mol的氢离子,1mol的氢离子得到1mol的电子,而1mol的转移3mol的电子,所以氧化剂和还原剂的物质的量之比为3:1,所以答案是:铝片,2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑,3:1;(3)上述实验说明,“直接利用金属活动性顺序表判断电池中的正负极”并不考可靠,最好是接一个电流计,通过观察电流方向判断原电池的正负极,所以答案是:不可靠;在两电极之间连上一个电流计测电流方向,判断原电池的正负极.

 智慧小复习系列答案
智慧小复习系列答案


