题目内容
【题目】某兴趣小组对铜与浓硫酸反应产生的黑色沉淀(可能含有CuO、CuS、Cu2S,其中CuS和 Cu2S不溶于稀盐酸、稀硫酸)进行探究,实验步骤如下:
Ⅰ.将光亮铜丝插人浓硫酸,加热;
Ⅱ.待产生大量黑色沉淀和气体时,抽出铜丝,停止加热;
Ⅲ.冷却后,从反应后的混合物中分离出黑色沉淀,洗净、干燥备用.
回答下列问题:
(1)步骤Ⅱ产生气体的化学式为 .
(2)向含微量 Cu2+试液中滴加K4[Fe(CN)6]溶液,能产生红褐色沉淀.现将少量黑色沉淀放入稀硫酸中,充分振荡以后,再滴加K4[Fe(CN)6]溶液,未见红褐色沉淀,由此所得结论是 .
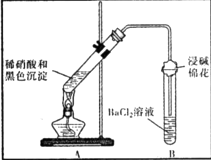
(3)为证明黑色沉淀含有铜的硫化物,进行如下实验:
装置 | 现象 | 结论及解释 |
| ①A试管中黑色沉淀逐渐溶解 | a.现象②说明褐色沉淀具有 |
(4)CuS固体能溶于热的浓硫酸,请用有关平衡移动原理加以解释: .
(5)为测定黑色沉淀中Cu2S 的百分含量,取0.2g 步骤Ⅰ所得黑色沉淀,在酸性溶液中用 40.0mL 0.075mol/L KMnO4溶液处理,发生反应如下:
8MnO4﹣+5Cu2S+44H+═10Cu2++5SO2↑+8Mn2++22H2O
6MnO4﹣+5CuS+28H+═5Cu2++5SO2↑+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2 , 过量的高锰酸钾溶液恰好与35.0mL 0.1mol/L (NH4)2Fe(SO4)2 溶液反应完全.则混合物中Cu2S 的质量分数为 .
【答案】
(1)SO2
(2)黑色沉淀中不含有CuO
(3)还原性;NO2+SO2+Ba2++H2O═BaSO4↓+NO↑+2H+
(4)CuS存在溶解平衡CuS(s)?Cu2+(aq)+S2﹣(aq),热的浓硫酸将S2﹣氧化,使S2﹣浓度减小,促进上述平衡向正向移动,使CuS溶解
(5)40%
【解析】解:(1.)Cu与浓硫酸反应生成硫酸铜、二氧化硫和水,反应为Cu+2H2SO4(浓) ![]() CuSO4+2SO2↑+2H2O,步骤Ⅱ产生的气体是SO2 , 故答案为:SO2;
CuSO4+2SO2↑+2H2O,步骤Ⅱ产生的气体是SO2 , 故答案为:SO2;
(2.)向试液中滴加K4[Fe(CN)6]溶液,若产生红褐色沉淀,证明有Cu2+ , 根据②将黑色沉淀放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,未见红褐色沉淀可知,黑色固体中一定不含CuO,故答案为:黑色沉淀中不含有CuO;
(3.)a、A试管内上方出现红棕色气体,说明反应中有一氧化氮生成,证明了黑色固体具有还原性,在反应中被氧化,故答案为:还原性;b、根据反应现象③B试管中出现白色沉淀可知,白色沉淀为硫酸钡,说明黑色固体中含有硫元素,发生反应的离子方程式为:NO2+SO2+Ba2++H2O═BaSO4↓+NO↑+2H+ , 故答案为:NO2+SO2+Ba2++H2O═BaSO4↓+NO↑+2H+;
(4.)CuS难溶于水,在水溶液中会有很少量的Cu溶解,溶液中存在沉淀溶解平衡,CuS(s)Cu2+(aq)+S2﹣(aq),热的浓硫酸将S2﹣氧化,使S2﹣浓度减小,促进上述平衡向正向移动,使CuS溶解;
故答案为:CuS存在溶解平衡CuS(s)Cu2+(aq)+S2﹣(aq),热的浓硫酸将S2﹣氧化,使S2﹣浓度减小,促进上述平衡向正向移动,使CuS溶解;
(5.)发生的反应为:
8MnO4﹣+5Cu2S+44H+═10Cu2++5SO2↑+8Mn2++22H2O
6MnO4﹣+5CuS+28H+═5Cu2++5SO2↑+6Mn2++14H2O
MnO4﹣+5Fe2++8H+═Mn2++5Fe3++4H2O
设Cu2S、CuS的物质的量分别为x、y,
与Cu2S、CuS反应后剩余KMnO4的物质的量:0.035L×0.1mol/L× ![]() =0.0007mol,
=0.0007mol,
160x+96y=0.2![]() +
+ ![]() =0.04×0.075﹣0.0007
=0.04×0.075﹣0.0007
解得x=0.0005mol,
Cu2S的质量分数: ![]() ×100%=40%,故答案为:40%.
×100%=40%,故答案为:40%.
(1)根据铜与浓硫酸反应生成二氧化硫气体进行解答;(2)根据题中信息中检验铜离子的方法对②进行分析,然后得出正确结论;(3)a、红棕色气体为二氧化氮,说明稀硝酸被还原生成一氧化氮,黑色固体具有还原性;
b、根据反应现象③可知黑色固体与稀硝酸反应生成了二氧化硫,证明黑色固体中含有硫元素;二氧化氮、二氧化硫的混合气体能够与氯化钡反应生成硫酸钡沉淀,据此写出反应的离子方程式;(4)CuS在溶液中存在沉淀溶解平衡,根据平衡移动分析;(5)依据滴定实验数据计算剩余高锰酸钾物质的量,得到和硫化亚铜、硫化铜反应的高锰酸钾物质的量,依据反应的离子方程式列式计算得到.

 星级口算天天练系列答案
星级口算天天练系列答案