题目内容
 某校化学研究性学习小组欲设计实验验证Al、Fe、Cu的金属活动性,他们提出了以下两种方案.请你帮助他们完成有关实验项目:
某校化学研究性学习小组欲设计实验验证Al、Fe、Cu的金属活动性,他们提出了以下两种方案.请你帮助他们完成有关实验项目:(1)用三种金属与盐酸反应的现象来判断,实验中除选择大小相同的金属片外,还需要控制
盐酸的浓度
盐酸的浓度
、溶液的温度
溶液的温度
相同;若选用一种盐溶液验证三种金属的活泼性,该试剂为硫酸亚铁溶液(或其他的亚铁盐溶液)
硫酸亚铁溶液(或其他的亚铁盐溶液)
.(2)①若用Fe、Cu作电极设计成原电池,以确定Fe、Cu的活动性.试在下面方框中画出原电池装置图,标出原电池的电极材料和电解质溶液.
上述装置中正极反应式为
2H++2e-=H2↑或Cu2++2e-=Cu
2H++2e-=H2↑或Cu2++2e-=Cu
.②某小组同学采用Al、Fe作为电极,只用一个原电池证明三种金属的活动性,则电解质溶液最好选用
D
D
.A.0.5mol?L-1氯化亚铁溶液 B.0.5mol?L-1氯化铜溶液
C.0.5mol?L-1盐酸 D.0.5mol?L-1氯化亚铁和0.5mol?L-1氯化铜混合溶液
(3)利用提供的试剂和用品:0.1mol?L-1盐酸溶液、0.1mol?L-1醋酸溶液、0.5mol?L-1氯化铝溶液、0.5mol?L-1氢氧化钠溶液、PH试纸.
请设计最简单实验证明氢氧化铝为弱碱
取适量的氯化铝溶液,用pH试纸测其pH值小于7,则证明氢氧化铝为弱碱
取适量的氯化铝溶液,用pH试纸测其pH值小于7,则证明氢氧化铝为弱碱
.分析:(1)用三种金属与盐酸反应的现象来判断金属的活泼性,实验中除选择大小相同的金属片外,温度、浓度等外界因素应相同,选择盐溶液时利用金属单质之间的置换反应比较金属的活泼性;
(2)①原电池中Fe为负极,Cu为正极,则Fe活泼性强,可选硫酸或硫酸铜作电解质;
②Al、Fe作为电极,只用一个原电池证明三种金属的活动性,由金属阳离子的得电子能力比较;
(3)测定盐溶液的pH可知对应的碱的碱性强弱.
(2)①原电池中Fe为负极,Cu为正极,则Fe活泼性强,可选硫酸或硫酸铜作电解质;
②Al、Fe作为电极,只用一个原电池证明三种金属的活动性,由金属阳离子的得电子能力比较;
(3)测定盐溶液的pH可知对应的碱的碱性强弱.
解答: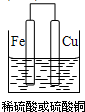 解:(1)用三种金属与盐酸反应的现象来判断金属的活泼性,实验中除选择大小相同的金属片外,温度、浓度等外界因素应相同,则盐酸的浓度、溶液的温度应相同,选择盐溶液时利用金属单质之间的置换反应比较金属的活泼性,则可选择硫酸亚铁溶液(或其他的亚铁盐溶液),Al可置换出Fe,而Cu不能,以此可知金属活泼性为Al>Fe>Cu,
解:(1)用三种金属与盐酸反应的现象来判断金属的活泼性,实验中除选择大小相同的金属片外,温度、浓度等外界因素应相同,则盐酸的浓度、溶液的温度应相同,选择盐溶液时利用金属单质之间的置换反应比较金属的活泼性,则可选择硫酸亚铁溶液(或其他的亚铁盐溶液),Al可置换出Fe,而Cu不能,以此可知金属活泼性为Al>Fe>Cu,
故答案为:盐酸的浓度;溶液的温度;硫酸亚铁溶液(或其他的亚铁盐溶液);
(2)①原电池中Fe为负极,Cu为正极,则Fe活泼性强,可选硫酸或硫酸铜作电解质,原电池装置如右图,正极反应为2H++2e-=H2↑或Cu2++2e-=Cu,故答案为:2H++2e-=H2↑或Cu2++2e-=Cu;
②Al、Fe作为电极,只用一个原电池证明三种金属的活动性,由金属阳离子的得电子能力比较,只有D符合,选D时铜离子先得到电子,然后亚铁离子得电子,由此可确定金属的活泼性,故答案为:D;
(3)测定盐溶液的pH可知对应的碱的碱性强弱,则最简单的实验方法为取适量的氯化铝溶液,用pH试纸测其pH值小于7,则证明氢氧化铝为弱碱,故答案为:取适量的氯化铝溶液,用pH试纸测其pH值小于7,则证明氢氧化铝为弱碱.
 解:(1)用三种金属与盐酸反应的现象来判断金属的活泼性,实验中除选择大小相同的金属片外,温度、浓度等外界因素应相同,则盐酸的浓度、溶液的温度应相同,选择盐溶液时利用金属单质之间的置换反应比较金属的活泼性,则可选择硫酸亚铁溶液(或其他的亚铁盐溶液),Al可置换出Fe,而Cu不能,以此可知金属活泼性为Al>Fe>Cu,
解:(1)用三种金属与盐酸反应的现象来判断金属的活泼性,实验中除选择大小相同的金属片外,温度、浓度等外界因素应相同,则盐酸的浓度、溶液的温度应相同,选择盐溶液时利用金属单质之间的置换反应比较金属的活泼性,则可选择硫酸亚铁溶液(或其他的亚铁盐溶液),Al可置换出Fe,而Cu不能,以此可知金属活泼性为Al>Fe>Cu,故答案为:盐酸的浓度;溶液的温度;硫酸亚铁溶液(或其他的亚铁盐溶液);
(2)①原电池中Fe为负极,Cu为正极,则Fe活泼性强,可选硫酸或硫酸铜作电解质,原电池装置如右图,正极反应为2H++2e-=H2↑或Cu2++2e-=Cu,故答案为:2H++2e-=H2↑或Cu2++2e-=Cu;
②Al、Fe作为电极,只用一个原电池证明三种金属的活动性,由金属阳离子的得电子能力比较,只有D符合,选D时铜离子先得到电子,然后亚铁离子得电子,由此可确定金属的活泼性,故答案为:D;
(3)测定盐溶液的pH可知对应的碱的碱性强弱,则最简单的实验方法为取适量的氯化铝溶液,用pH试纸测其pH值小于7,则证明氢氧化铝为弱碱,故答案为:取适量的氯化铝溶液,用pH试纸测其pH值小于7,则证明氢氧化铝为弱碱.
点评:本题以金属活泼性的比较为载体考查原电池,明确金属的活泼性及原电池的工作原理即可解答,注重基础知识和学生迁移能力的考查,题目难度中等.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
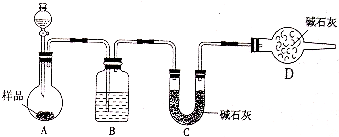

 某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.
某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.