题目内容
8.若反应N2+3H2=2NH3在某温度下的平衡常数为K1,而反应NH3=$\frac{1}{2}$N2+$\frac{3}{2}$H2在该温度下的平衡常数为K2,则K1和K2的关系为K1=$\frac{1}{{K}_{2}^{2}}$.分析 化学平衡状态是可逆反应在该条件下进行的最大限度,平衡常数就是平衡状态的一种数量标志,是表明化学反应限度的一种特征值. 化学平衡常数通常用各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值来表示,所以N2+3H2=2NH3,平衡常数K1=$\frac{{c}^{2}(N{H}_{3})}{{c}^{3}({H}_{2})•c({N}_{2})}$;氨的合成反应NH3=$\frac{1}{2}$N2+$\frac{3}{2}$H2 的平衡常数根据平衡常数K2=$\frac{{c}^{1.5}({H}_{2})•{c}^{0.5}({N}_{2})}{c(N{H}_{3})}$,分析解答.
解答 解:化学平衡状态是可逆反应在该条件下进行的最大限度,平衡常数就是平衡状态的一种数量标志,是表明化学反应限度的一种特征值. 化学平衡常数通常用各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值来表示,所以N2+3H2=2NH3,平衡常数K1=$\frac{{c}^{2}(N{H}_{3})}{{c}^{3}({H}_{2})•c({N}_{2})}$;氨的合成反应NH3=$\frac{1}{2}$N2+$\frac{3}{2}$H2 的平衡常数根据平衡常数K2=$\frac{{c}^{1.5}({H}_{2})•{c}^{0.5}({N}_{2})}{c(N{H}_{3})}$,所以K1=$\frac{1}{{K}_{2}^{2}}$,故答案为:K1=$\frac{1}{{K}_{2}^{2}}$.
点评 本题考查了有关化学平衡常数的计算,注意化学平衡常数是指生成物浓度的系数次幂之积与反应物浓度系数次幂之积的比值,题目难度不大.

 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案| A. | R位于元素周期表中的第VA族 | B. | R位于元素周期表中的第 VIIA族 | ||
| C. | RO3-中的R元素只能被还原 | D. | R2在常温常压下一定是气体 |
| A. | 配制标准溶液的NaOH中混有Na2CO3杂质 | |
| B. | 滴定终点读数时,俯视滴定管的刻度,其他操作正确 | |
| C. | 盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗 | |
| D. | 滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液 |
| A. | Na2CO3固体 | B. | NaCl溶液 | C. | 浓H2SO4 | D. | KNO3溶液 |
| A. | s区 | B. | d区 | C. | f区 | D. | ds区 |
(1)A在周期表中的位置是第一周期ⅠA族,
(2)由这些元素组成的物质,其组成和结构信息如表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为BDF2 |
b的化学式为Na2O2和Na2C2(写一种即可);
c的电子式为
 .
. 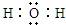 ,C和D形成的一种化合物与A2C发生氧化还原反应,该反应的离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑
,C和D形成的一种化合物与A2C发生氧化还原反应,该反应的离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑
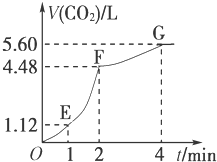 向200mL 6mol/L的盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准状况下测定)请回答下列问题:
向200mL 6mol/L的盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准状况下测定)请回答下列问题: