题目内容
【题目】工业废水随意排放会造成严重污染,根据成分不同可采用不同的处理方法.
(1)电池生产工业废水中常含有Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去.已知室温下Ksp(FeS)=6.3×10﹣18mol2L﹣2 , Ksp(CuS)=1.3×10﹣36mol2L﹣2 . ①请用离子方程式说明上述除杂的原理 .
②FeS高温煅烧产生的SO2气体通入下列溶液中,能够产生沉淀的是(填序号)
A.Ba(NO3)2B.BaCl2
C.Ba(OH)2D.溶有NH3的BaCl2溶液
③已知元素在高价态时常表现氧化性,若在酸性CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀,则生成CuCl的离子方程式是 .
(2)电解法处理酸性含铬废水(主要含有Cr2O72﹣)时,在废水中加入适量NaCl,以铁板作阴、阳极,处理过程中存在如下反应Cr2O72+6Fe2++14H+═2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确的是(填序号)
A.阳极反应为Fe﹣2e﹣═Fe2+
B.电解过程中溶液pH减小
C.过程中有Fe(OH)3沉淀生成
D.电路中每转移12 mol电子,最多有2mol Cr2O72﹣被还原
(3)废氨水可以转化成氨,氨再设计成碱性燃料电池.图是该燃料电池示意图,产生的X气体可直接排放到大气中,a电极作极(填“正”“负”“阴”或“阳”),其电极反应式为 . 
【答案】
(1)FeS(s)+Cu2+(aq)=CuS(s)+Fe2+(aq);ACD;2Cu2++SO32﹣+2Cl﹣+H2O ![]() 2CuCl↓+SO42﹣+2H+
2CuCl↓+SO42﹣+2H+
(2)BD
(3)负;2NH3+6OH﹣﹣6e﹣=N2+6H2O
【解析】解:(1)①由于Ksp(FeS)>Ksp(CuS),所以在相同条件下CuS的溶解度更小,沉淀会向着生成CuS的方向进行,故离子方程式为FeS(s)+Cu2+(aq)=CuS(s)+Fe2+(aq),所以答案是:①FeS(s)+Cu2+(aq)=CuS(s)+Fe2+(aq);②A、Ba(NO3)2 中有硝酸根离子,二氧化硫通入后生成亚硫酸,亚硫酸电离出氢离子,就相当于硝酸了.硝酸氧化亚硫酸成硫酸,硫酸根离子和钡离子结合生成硫酸钡沉淀,故可选;
B、因为亚硫酸钡溶于盐酸,较弱酸不能制备较强酸,所以不能生成沉淀,故不可选;
C、二氧化硫和氢氧根反应生成亚硫酸根离子,钡离子和亚硫酸根离子结合生成亚硫酸钡沉淀,故可选;
D、与B项相比,溶有氨气的BaCl2溶液呈碱性,在碱性溶液中可以生成亚硫酸钡沉淀,故可选;
所以答案是:ACD;③已知元素在高价态时常表现氧化性,若在酸性CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀,则生成CuCl的离子方程式为:2Cu2++SO32﹣+2Cl﹣+H2O ![]() 2CuCl↓+SO42﹣+2H+ , 所以答案是:2Cu2++SO32﹣+2Cl﹣+H2O
2CuCl↓+SO42﹣+2H+ , 所以答案是:2Cu2++SO32﹣+2Cl﹣+H2O ![]() 2CuCl↓+SO42﹣+2H+;(2)A.Fe板作阳极,为活性电极,Fe失电子,发生氧化反应生成亚铁离子,阳极反应为Fe﹣2e﹣═Fe2+ , 故A正确;
2CuCl↓+SO42﹣+2H+;(2)A.Fe板作阳极,为活性电极,Fe失电子,发生氧化反应生成亚铁离子,阳极反应为Fe﹣2e﹣═Fe2+ , 故A正确;
B.由反应式Cr2O72﹣+6Fe2++14H+═2Cr3++6Fe3++7H2O可知,处理过程中消耗氢离子,溶液的酸性减弱,溶液pH增大,故B错误;
C.阴极发生还原反应,溶液中的氢离子得到电子减少,同时生成氢氧根,有Fe(OH)3沉淀生成,故C正确;
D.Fe﹣2e﹣=Fe2+ , 则转移电子数12mol需要6molFe,再根据能够处理的关系式,得6Fe~12e﹣~6Fe2+~Cr2O72﹣ , 故被还原的Cr2O72﹣的物质的量为1mol,故D错误;
故选BD;(3)在燃料电池中,可燃物充入负极区,所以NH3充入的a极作负极;产生的X气体为氧化产物,可直接排放到大气中,说明X对大气无污染,因此X为氮气,由该燃料电池示意图可知负极反应产物有水,由于是碱性电池,氢氧根离子也参与负极电极反应,综上所述可写出负极反应式:2NH3+6OH﹣﹣6e﹣=N2+6H2O;所以答案是:负;2NH3+6OH﹣﹣6e﹣=N2+6H2O.

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案【题目】下图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
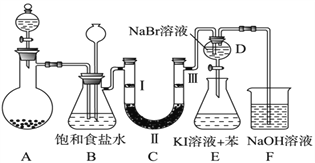
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:______。装置B中饱和食盐水的作用是________________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象__________________。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入_______。
a | b | c | d | |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |


