题目内容
【题目】W、X、Y、Z是原子序数依次增大的前四周期元素,W、Y在地壳中的含量处于前两位,X是周期表中电负性最大的元素,基态Z原子的价层电子数为8,下列说法正确的是
A.最高化合价:X>W>Y
B.Y与W、Y与X形成的二元化合物晶体类型相同
C.单质X在一定条件下能置换出单质W
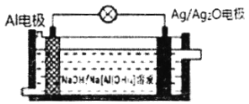
D.Z与W两种元素形成的常见化合物均为黑色固体
【答案】C
【解析】
W、X、Y、Z是原子序数依次增大的前四周期元素,由W、Y在地壳中的含量处于前两位可知,W为O元素、Y为Si元素,由X是周期表中电负性最大的元素可知,X是F元素,由基态Z原子的价层电子数为8可知,Z为Fe元素。
A.![]() 元素没有正价,
元素没有正价,![]() 元素最高价为+4,故A错误;
元素最高价为+4,故A错误;
B.![]() 是原子晶体,
是原子晶体,![]() 是分子晶体,晶体类型不同,故B错误;
是分子晶体,晶体类型不同,故B错误;
C. F元素的非金属性强于O元素,![]() 可与水反应置换出
可与水反应置换出![]() ,故C正确;
,故C正确;
D.铁的常见氧化物中![]() 为红棕色固体,故D错误;
为红棕色固体,故D错误;
故选C。

 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
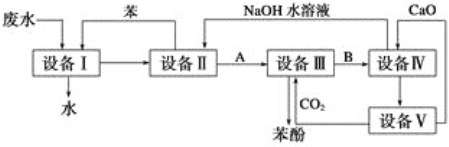
倍速训练法直通中考考点系列答案【题目】用酸性KMnO4溶液与H2C2O4(草酸)溶液反应研究影响反应速率的因素,一实验小组欲通过测定单位时间内生成CO2的体积,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化),实验装置如图所示:
实验序号 | A溶液 | B溶液 |
① | 20mL 0.1mol·L-1H2C2O4溶液 | 30mL 0.01mol·L-1KMnO4溶液 |
② | 20mL 0.2mol·L-1H2C2O4溶液 | 30mL 0.01mol·L-1KMnO4溶液 |

(1)写出该反应的离子方程式__________________________________________。
(2)该实验探究的是________因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是______>______(填实验序号)。
(3)若实验①在2min末收集了4.48mL CO2(标准状况下),则在2min末,c(MnO4-)=______ mol·L-1(假设混合溶液的体积为50mL)。
(4)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定_________________________来比较化学反应速率。
(5)小组同学发现反应速率变化如图,其中t1-t2时间内速率变快的主要原因可能是:①反应放热,②___________________。

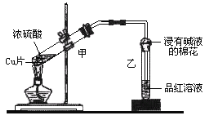
【题目】Ⅰ.实验室制得气体中常含有杂质,影响其性质检验。下图A为除杂装置,B为性质检验装置,完成下列表格:

序号 | 气体 | 反应原理 | A中试剂 |
① | 乙烯 | 溴乙烷和NaOH的醇溶液加热 | _________ |
② | 乙烯 | 无水乙醇在浓硫酸的作用下加热至170℃反应的化学方程式是________________。 | NaOH溶液 |
③ | 乙炔 | 电石与饱和食盐水反应 | _________ |
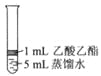
Ⅱ.为探究乙酸乙酯的水解情况,某同学取大小相同的3支试管,分别加入以下溶液,充分振荡,放在同一水浴加热相同时间,观察到如下现象。
试管编号 | ① | ② | ③ |
实验操作 |
|
|
|
实验现象 | 酯层变薄 | 酯层消失 | 酯层基本不变 |
(1)试管①中反应的化学方程式是_____________________;
(2)对比试管①和试管③的实验现象,稀H2SO4的作用是________________;
(3)试用化学平衡移动原理解释试管②中酯层消失的原因_______________。