题目内容
3.下列物质在一定条件下可与甲烷发生反应的是( )| A. | 氯气 | B. | 溴水 | ||
| C. | 氢氧化钠溶液 | D. | 酸性高锰酸钾溶液 |
分析 甲烷是正四面体结构,甲烷分子中每个原子都达到稳定结构,所以甲烷性质稳定,不与强酸、强碱、强氧化剂反应,能够与氯气在光照条件下发生取代反应,据此解答.
解答 解:A.甲烷在光照条件下与氯气发生取代反应,故A正确;
B.甲烷性质稳定与溴水不反应,故B错误;
C.甲烷性质稳定不能与氢氧化钠溶液反应,故C错误;
D.甲烷不能被酸性高锰酸钾氧化,故D错误;
故选:A.
点评 本题考查了甲烷的化学性质,熟悉甲烷结构是解题关键,题目难度不大,注意对基础知识的积累.

练习册系列答案
相关题目
14.下列实验装置与叙述正确的是( )
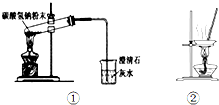

| A. | 用图①所示装置做碳酸氢钠固体受热分解实验 | |
| B. | 用装置②蒸干氯化镁溶液制MgCl2•6H2O | |
| C. | 锥形瓶可用作加热的反应器,滴定时不得用待测溶液润洗 | |
| D. | 配制溶液定容时,俯视容量瓶刻度会使溶液浓度偏低 |
11.下列各组物质中,都是强电解质的是( )
| A. | HBr、Cu(OH)2、BaSO4 | B. | NaOH、Ca(OH)2、NH3•H2O | ||
| C. | HClO、NaF、Ba(OH)2 | D. | NH4Cl、CH3COONa、Na2S |
8.对于反应4NH3+5O2?4NO+6H2O,下列为四种不同情况下测得的反应速率,其中能表明该反应进行最快的是( )
| A. | v (NH3)=0.2 mol/(L•s) | B. | v (O2)=1.4mol/(L•min) | ||
| C. | v (H2O)=0.25 mol/(L•s) | D. | v (NO)=0.9 mol/(L•min) |
12.在0.1mol•L-1CH3COOH溶液中存在如下电离平衡:CH3COOH?CH3COO-+H+,对于该平衡,下列叙述正确的是( )
| A. | 加入少量CH3COONa固体,平衡向正反应方向移动 | |
| B. | 加入少量NaOH固体,平衡向正反应方向移动 | |
| C. | 通入少量HCl气体,溶液中pH值增大 | |
| D. | 加入水时,平衡向逆反应方向移动 |
13.已知H2CO3?H++HCO${\;}_{3}^{-}$,K1=4.3×10-7,HCO3-?H++CO32-,K2=5.6×10-11;HClO?H++ClO-,K=3.0×10-8,根据上述电离常数分析,下列各式中错误的是( )
| A. | Ca(ClO)2+2HCl═CaCl2+2HClO | B. | Ca(ClO)2+2H2O+2CO2═Ca(HCO3)2+2HCl | ||
| C. | NaClO+H2O+CO2═NaHCO3+HClO | D. | 2NaClO+H2O+CO2═Na2CO3+2HClO |