题目内容
【题目】下列实验现象预测正确的是( )
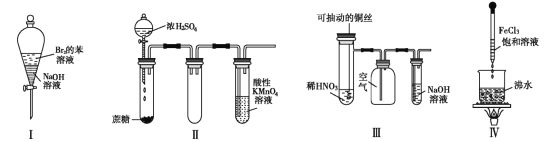
A. 实验Ⅰ:振荡后静置,上层溶液颜色保持不变
B. 实验Ⅱ :酸性 KMnO4 溶液中出现气泡,且颜色逐渐褪去
C. 实验Ⅲ:微热稀 HNO3 片刻,溶液中有气泡产生,广口瓶内始终保持无色
D. 实验Ⅳ:滴入 FeCl3 后,可形成带电的胶体,该分散系导电能力增强
【答案】B
【解析】A.根据单质溴能与NaOH溶液发生反应,苯与水互不相溶;B.根据浓硫酸具有脱水性和氧化性的性质分析;C.根据在加热时稀硝酸与铜发生反应,硝酸被还原成NO,广口瓶内有空气,可与NO反应;D.胶体粒子带电荷,胶体本身不带电。
A项,苯的密度比水小,位于上层,苯中的Br2与NaOH溶液发生反应,因此振荡后静置,上层溶液褪色,故A项错误;
B项,浓H2SO4与蔗糖发生氧化还原反应生成SO2和CO2,CO2不与酸性KMnO4溶液反应,有气泡产生,SO2与酸性KMnO4溶液发生氧化还原反应使溶液褪色,故B项正确;
C项,微热稀HNO3片刻,铜与稀HNO3发生反应生成NO,NO与广口瓶内的O2反应生成红棕色的NO2,故C项错误。
D项,FeCl3饱和溶液滴入沸水中继续煮沸至红褐色,生成氢氧化铁胶体,胶体电中性,不带电,故D项错误;
综上所述,本题正确答案为B。

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案【题目】某学生为了探究影响化学反应速率的外界因素,进行以下实验。
(1)向100mL稀硫酸中加入过量的锌粉,标准状况下测得数据累计值如下:
时间/min | 1 | 2 | 3 | 4 | 5 |
氢气体积/mL | 50 | 120 | 232 | 290 | 310 |
①在0~1、1~2、2~3、3~4、4~5min各时间段中:
反应速率最大的时间段是________min,主要的原因可能是_____________________;
反应速率最小的时间段是________min,主要的原因可能是_____________________。
②为了减缓反应速率但不减少产生氢气的量,可以在稀硫酸中加入________(填序号)。
a.蒸馏水 b.NaOH溶液 c.NaNO3溶液 d.Na2CO3溶液
(2)进行以下对比实验并记录实验现象。
实验 Ⅰ
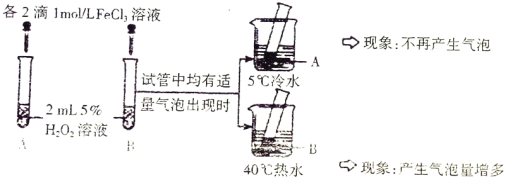
实验 Ⅱ:另取两支试管分别加入5mL5%eH2O2溶液和5mL10%H2O2溶液,均未观察到有明显的气泡
产生。
①双氧水分解的化学方程式是________________。
②实验 Ⅰ 的目的是______________。
③实验 Ⅱ 未观察到预期现象,为了达到该实验的目的,可采取的改进措施是__________________。