题目内容
【题目】红磷P(s)和 Cl2 发生反应生成 PCl3 和 PCl5,反应过程和能量关系如图所示。△H 表示生成 1mol产物的焓变数据。下列热化学方程式不正确的是
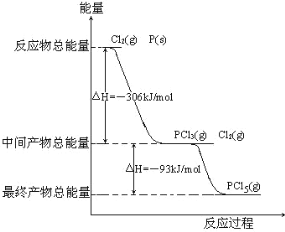
A.2P (s)+3Cl2 (g)=2PCl3 (g) △H=-612kJ·mol-1
B.PCl3 (g) =P (g)+ ![]() Cl2 (g) △H=306kJ·mol-1
Cl2 (g) △H=306kJ·mol-1
C.PCl5 (g)=PCl3 (g)+Cl2 (g) △H=93kJ·mol-1
D.2P (s)+5Cl2 (g)=2PCl5 (g) △H=-798kJ·mol-1
【答案】B
【解析】
A.P和Cl2反应生成PCl3的热化学方程式为P(s)+![]() Cl2(g)═PCl3(g) △H=-306 kJ/mol,则2P (s)+3Cl2 (g)=2PCl3 (g) △H=-612kJ·mol-1,故A正确;
Cl2(g)═PCl3(g) △H=-306 kJ/mol,则2P (s)+3Cl2 (g)=2PCl3 (g) △H=-612kJ·mol-1,故A正确;
B.P和Cl2反应生成PCl3的热化学方程式为P(s)+![]() Cl2(g)═PCl3(g) △H=-306 kJ/mol,则PCl3 (g) =P (s)+
Cl2(g)═PCl3(g) △H=-306 kJ/mol,则PCl3 (g) =P (s)+ ![]() Cl2 (g) △H=306kJ·mol-1,生成的P应该为固体,故B错误;
Cl2 (g) △H=306kJ·mol-1,生成的P应该为固体,故B错误;
C.其他条件不变,对于PCl5分解生成PCl3和Cl2的反应,热化学方程式为PCl5(g)=PCl3(g)+Cl2(g);△H=+93 kJ/mol,故C正确;
D.根据图中数据,可得P(s)+![]() Cl2(g)=PCl5(g) △H=-399kJ/mol,则有反应2P(s)+5Cl2(g)═2PCl5(g)对应的反应热△H=-798kJmol-1,故D正确;
Cl2(g)=PCl5(g) △H=-399kJ/mol,则有反应2P(s)+5Cl2(g)═2PCl5(g)对应的反应热△H=-798kJmol-1,故D正确;
故选B。

 名校课堂系列答案
名校课堂系列答案【题目】碘在科研与生活中有重要应用。
(1)I2O5 是白色粉末状固体,在合成氨工业中常用 I2O5 来定量测量 CO 的含量。
已知:2I2 (s)+5O2 (g)=2I2O5 (s) △H=﹣75.56kJ·mol-1
2CO (g)+O2 (g)=2CO2 (g) △H=﹣566.0kJ·mol-1
写出 CO (g)与 I2O5 (s)反应析出固态 I2 的热化学方程式:_____,若这个反应一定能自发进行,则反应的△S_____0(填“>”,“<”或 “=”);
(2)某兴趣小组用 0.50mol·L-1KI、0.2%淀粉溶液、0.20mol·L-1K2S2O8、0.10mol·L-1Na2S2O3 等试 剂,探究反应条件对化学反应速率的影响。
已知:Ⅰ、S2O82-+2I-=2SO42-+I2(慢) Ⅱ、I2+2S2O32-=2I- +S4O62-(快)
①向 KI、Na2S2O3 与淀粉的混合溶液中加入一定量的 K2S2O8 溶液,当溶液中的_____耗 尽后,溶液颜色将由无色变成为蓝色。 请从碰撞理论的角度解释上述产物未耗尽前溶液中看不到蓝色的原因:_____
②为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验 序号 | 体积 V/mL | ||||
K2S2O8 溶液 | 水 | KI 溶液 | Na2S2O3 溶液 | 淀粉溶液 | |
ⅰ | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
ⅱ | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
ⅲ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
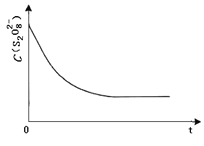
表中 Vx=_____mL,理由是_____。
③已知某条件下,浓度 c (S2O82-)~反应时间 t 的变化曲线如图,若保持其他条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时 c (S2O82-)~t 的变化曲线示意图 _____(进行相应的标注)