��Ŀ����
��X��Y��Z��W���ֶ�����Ԫ�أ�ԭ����������������˵�����ܺ�Ϊ38��YԪ��ԭ������������ռ��������������3/4��WԪ��ԭ��������������ͬ����ZԪ�ض�5�����ӣ�W��Y������ͬһ���塣?(1)��д��Ԫ�ط��ţ�X?��������?��Y?��������?��Z?��������?��W?��������?�� (2)Z��W��Ԫ�ص�����������Ӧ��ˮ���ﷴӦ�ķ���ʽ��������������������������?
(3)��Z�ĵ���(Ƭ״)������з�̪�ķ�ˮ�У��۲쵽������������������������������Ӧ�Ļ�ѧ����ʽ������������������������������������
(1)H��O��Mg��Cl?
(2)Mg(OH)2+2HClO4![]() Mg(ClO4)2+2H2O?
Mg(ClO4)2+2H2O?
(3)��Һ��죬�����ݲ�����Mg+2H2O![]() Mg(OH)2+H2��?
Mg(OH)2+H2��?
��������Y������������Ϊx��![]() ��x=6������YΪO����X��Y��Z��Wԭ����������������W��Z��5������(ͬһ����)��������5�����ӣ���ԭ��������5����(2)��Ҫ��Z��W����۲�ֵΪ5����A���A���A���A��W����Bͬ���壬ֻ��Mg��Cl���ϡ�?
��x=6������YΪO����X��Y��Z��Wԭ����������������W��Z��5������(ͬһ����)��������5�����ӣ���ԭ��������5����(2)��Ҫ��Z��W����۲�ֵΪ5����A���A���A���A��W����Bͬ���壬ֻ��Mg��Cl���ϡ�?
�ɵ�(3)��ѵ���Z(Ƭ״)ҪͶ�뵽��ˮ�з�Ӧ��Zֻ��ΪMg���ʣ�����ZΪMg��WΪ�ȣ�X��ΪH(

��ϰ��ϵ�д�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
�����Ŀ

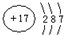

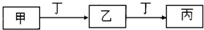
 ��X��Y��Z��W���ֶ�����Ԫ�أ�ԭ��������������X�������Ӿ���һ�����ӣ�Z��W�����ڱ��ڴ���ͬһ��������λ�ã����ǵĵ�����ͨ��״���¾�Ϊ��ɫ���壮Yԭ�ӵ������������Ǵ�����������2������ش�
��X��Y��Z��W���ֶ�����Ԫ�أ�ԭ��������������X�������Ӿ���һ�����ӣ�Z��W�����ڱ��ڴ���ͬһ��������λ�ã����ǵĵ�����ͨ��״���¾�Ϊ��ɫ���壮Yԭ�ӵ������������Ǵ�����������2������ش�