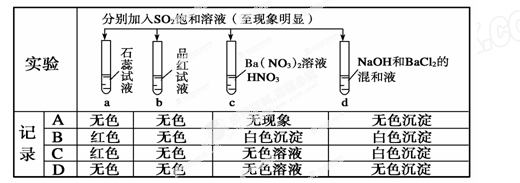
题目内容
已知KMnO4与浓盐酸在常温下反应能产生Cl2。若用下图所示的实验装置来制备纯净、干燥的氯气,并试验它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是…( )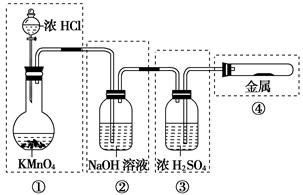
| A.①和②处 | B.②处 | C.②和③处 | D.②③④处 |
D
解析试题分析:②错,应装饱和NaCl溶液,除HCl;若用NaOH溶液,除Cl2,无法进行性质实验。③错,导管应长进短出。④错,反应应加热,反应应在直管内进行,多余的氯气,从直管的另一端出,用NaOH溶液吸收。选D。
考点:考查氯气的实验室制法和性质实验等相关知识。

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
下列块状金属在常温下能全部溶于足量的浓硝酸的是
| A.Au | B.Cu | C.Fe | D.Al |
能证明碳酸比硅酸酸性强的实验事实是
| A.H2CO3比H2SiO3受热易分解 |
B.高温下能发生反应Na2CO3+SiO2 Na2SiO3+CO2↑ Na2SiO3+CO2↑ |
| C.CO2能溶于水生成碳酸,而SiO2却不溶于水 |
| D.CO2通入Na2SiO3溶液中有胶状沉淀生成 |
下列关于硅元素的说法,不正确的是
| A.光导纤维的主要成分是二氧化硅 | B.二氧化硅可以和水直接反应来制取硅酸 |
| C.硅可用作太阳能电池 | D.硅酸钠是制备硅胶和木材防火剂等的原料 |
下列说法正确的是( )
| A.硫粉在过量的氧气中燃烧可以生成SO3 |
| B.可以用澄清石灰水鉴别CO2和SO2 |
| C.将少量CO2通入BaCl2溶液能生成白色沉淀 |
| D.不能用排水法收集SO2、NO2气体 |
下列陈述正确并且有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | 浓硫酸有强氧化性 | 浓硫酸可用于干燥H2和CO |
| D | Fe3+有强氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |