题目内容
【题目】近几年来关于氮污染的治理倍受关注。
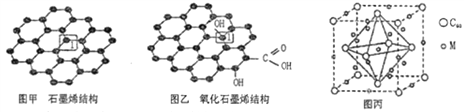
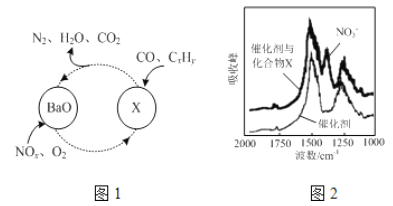
(1)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、CxHy、NOx三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
①在图示的转化中,被还原的元素是_______________,X的化学式为__________________。
②钡元素在周期表中的位置是___________________________。
(2)SCR技术可使NOx与NH3直接反应,实现无害转化。当NO与NO2的物质的最之比为2:1时,写出发生反应的化学方程式:____________________________。
(3)利用ClO2氧化氮氧化物反应过程如下:NO![]() NO2
NO2![]() N2反应I的化学方程式是2NO+ ClO2+H2O==NO2+HNO3+ 2HCl,反应II的离子方程式是__________________。
N2反应I的化学方程式是2NO+ ClO2+H2O==NO2+HNO3+ 2HCl,反应II的离子方程式是__________________。
(4)加入过量次氯酸钠可使废水中NH4+完全转化为N2,而本身被还原为NaCl。
①检验废水中是否存在NH4+的方法是_______________________________________________。
②若处理废水产生了0.448LN2 (标准状况),则需消耗浓度为2mol/L的次氯酸钠的体积为____mL。
【答案】 N、O Ba(NO3)2 第六周期第 IIA 族 16NH3+12NO+6NO2=17N2+24H2O 2NO2+4SO32-=N2+4SO42- 少量反应后A中溶液于试管中,向其中加入浓NaOH溶液,加热,用湿润的红色石蕊试纸接近试管口,若试紙变蓝,则A中生成NH4+ 30
【解析】(1) ①在图示的转化中N、O的化合价降低被还原;由傅里叶红外光谱图(如图2所示)确定化合物X含有硝酸根,在结合图1有钡离子参加,所以X的化学式为Ba(NO3)2;
②钡元素在周期表中的位置是第六周期第 IIA 族;
(2)因为NOx与NH3直接反应,实现无害转化,则生成氮气和水,所以当NO与NO2的物质的最之比为2:1时,发生反应的化学方程式为16NH3+12NO+6NO2=17N2+24H2O;因此,本题正确答案为:16NH3+12NO+6NO2=17N2+24H2O;
(3)二氧化氮具有氧化性,亚硫酸钠具有还原性,二者会发生氧化还原反应,因此,反应II的离子方程式是2NO2+4SO32-=N2+4SO42-;
(4)①检验NH4+的方法是:取少量反应后A中溶液于试管中,向其中加入浓NaOH溶液,加热,用湿润的红色石蕊试纸接近试管口,若试紙变蓝,则A中生成NH4+;
②因为次氯酸钠氧化废水中NH4+完全转化为N2,而本身被还原为NaCl,根据得失电子守恒,离子方程式:2NH4++3ClO-=N2↑+3Cl-+2H++3H2O 由2NH4++3ClO-=N2↑+3Cl-+2H++3H2O
知处理废水产生了0.448L氮气,即![]() =0.02mol,则需消耗浓度为2mol/L的次氯酸钠的体积为
=0.02mol,则需消耗浓度为2mol/L的次氯酸钠的体积为![]() ×1000mL=30mL;因此,本题正确答案为:30
×1000mL=30mL;因此,本题正确答案为:30

 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案