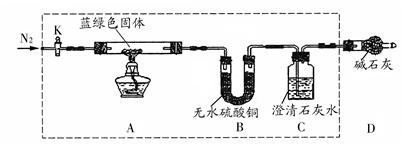
题目内容
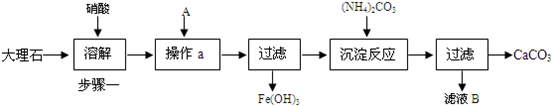
卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子.以卤块为原料可制得轻质氧化镁,工艺流程如图:
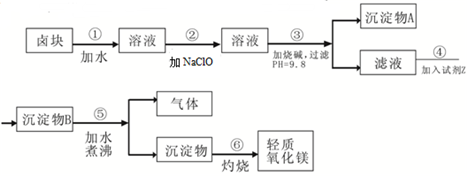
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe3+,生成Fe(OH)3沉淀除去.若要求产品尽量不含杂质,请根据表1表2提供的资料,填写空白:
表1生成氢氧化物沉淀的pH
表2化学试剂价格表
(1)在步骤②中加入漂液而不是双氧水其原因是______.写出加入NaClO发生反应的离子方程式______.
(2)在步骤③中控制pH=9.8,其目的是______.
(3)沉淀物A的成分为,试剂Z应该是______.
(4)在步骤⑤中发生反应的化学方程式是______.
(5)若在实验室中完成步骤⑥,则沉淀物必需在______(填仪器名称)中灼烧.

已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe3+,生成Fe(OH)3沉淀除去.若要求产品尽量不含杂质,请根据表1表2提供的资料,填写空白:
表1生成氢氧化物沉淀的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
| 试剂 | 价格(元/吨) |
| 漂液(含NaClO,25.2%) | 450 |
| 双氧水(含H2O2,30%) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
(2)在步骤③中控制pH=9.8,其目的是______.
(3)沉淀物A的成分为,试剂Z应该是______.
(4)在步骤⑤中发生反应的化学方程式是______.
(5)若在实验室中完成步骤⑥,则沉淀物必需在______(填仪器名称)中灼烧.
(1)步骤②是为了将Fe2+氧化成Fe3+,并在控制合适的pH条件时生成Fe(OH)3沉淀而除之.虽然漂液和H2O2都可采用,但对比表2提供的原料价格可以看出,漂液比H2O2的价格低得多,所以选漂液最合理,流程中加入次氯酸钠在酸性溶液中会氧化亚铁离子为铁离子,反应的离子方程式为:2Fe2++ClO-+2H+=2Fe3++Cl-+H2O;
故答案为:漂液比H2O2的价格低得多;2Fe2++ClO-+2H+=2Fe3++Cl-+H2O;
(2)步骤③的目的在于使除Mg2+以外的各种杂质金属离子都生成氢氧化物沉淀,以便通过过滤而除去,应加入NaOH,如加入纯碱,不能达到较高的PH,分析表1提供的数据:除去杂质离子合理的pH范围是3.7<pH<9.8,在此范围内,如果pH过高,就会有大量的Mg2+生成Mg(OH)2而进入沉淀中,从而导致生产成本的提高.为了兼顾产品质量和生产成本,选择pH=9.8最合理,当然此时Mg2+也会部分生成Mg(OH)2沉淀,但由于卤块价格低廉,这点不可避免的损失还是可以承受的,以此保证产品的纯度,
故答案为:使除Mg2+以外的各种杂质金属离子都成为氢氧化物沉淀以便除去;
(3)由流程分析可知,步骤②加入次氯酸钠是氧化剂,氧化亚铁离子为铁离子,调节溶液pH=9.8,依据图表数据判断形成沉淀的离子为Fe3+,Mn2+,Mg2+,反应形成的沉淀A为Fe(OH)3、Mn(OH)2、Mg(OH)2 ;步骤④的目的是将Mg2+从溶液中沉淀出来.从MgCl2制得MgO,有两种可行的方法,一种是向溶液中加入烧碱,另一种方法是向溶液中加入纯碱,此处选用后一种方法更合理.一方面,加烧碱生成的中间产物Mg(OH)2是胶状沉淀,会造成过滤困难,更重要的是反应过程中不能进行轻化处理,只能得到重质氧化镁;加纯碱生成的中间产物MgCO3呈粗颗粒状,易过滤,MgCO3在水中经一段时间的加热会有部分反应生成CO2,由于CO2气体的产生,使沉淀变得疏松,灼烧沉淀后得到的是轻质氧化镁.另一方面,对比表2中烧碱和纯碱的价格可以看出,纯碱比烧碱价格低得多,采用纯碱路线既合理又经济,
故答案为:Fe(OH)3、Mn(OH)2、Mg(OH)2;纯碱;
(4)步骤⑤中反应的化学方程式为MgCO3+H2O
Mg(OH)2+CO2↑,故答案为:MgCO3+H2O
Mg(OH)2+CO2↑;
(5)在实验室中完成步骤⑥,则沉淀物在坩埚中加热,故答案为:坩埚.
故答案为:漂液比H2O2的价格低得多;2Fe2++ClO-+2H+=2Fe3++Cl-+H2O;
(2)步骤③的目的在于使除Mg2+以外的各种杂质金属离子都生成氢氧化物沉淀,以便通过过滤而除去,应加入NaOH,如加入纯碱,不能达到较高的PH,分析表1提供的数据:除去杂质离子合理的pH范围是3.7<pH<9.8,在此范围内,如果pH过高,就会有大量的Mg2+生成Mg(OH)2而进入沉淀中,从而导致生产成本的提高.为了兼顾产品质量和生产成本,选择pH=9.8最合理,当然此时Mg2+也会部分生成Mg(OH)2沉淀,但由于卤块价格低廉,这点不可避免的损失还是可以承受的,以此保证产品的纯度,
故答案为:使除Mg2+以外的各种杂质金属离子都成为氢氧化物沉淀以便除去;
(3)由流程分析可知,步骤②加入次氯酸钠是氧化剂,氧化亚铁离子为铁离子,调节溶液pH=9.8,依据图表数据判断形成沉淀的离子为Fe3+,Mn2+,Mg2+,反应形成的沉淀A为Fe(OH)3、Mn(OH)2、Mg(OH)2 ;步骤④的目的是将Mg2+从溶液中沉淀出来.从MgCl2制得MgO,有两种可行的方法,一种是向溶液中加入烧碱,另一种方法是向溶液中加入纯碱,此处选用后一种方法更合理.一方面,加烧碱生成的中间产物Mg(OH)2是胶状沉淀,会造成过滤困难,更重要的是反应过程中不能进行轻化处理,只能得到重质氧化镁;加纯碱生成的中间产物MgCO3呈粗颗粒状,易过滤,MgCO3在水中经一段时间的加热会有部分反应生成CO2,由于CO2气体的产生,使沉淀变得疏松,灼烧沉淀后得到的是轻质氧化镁.另一方面,对比表2中烧碱和纯碱的价格可以看出,纯碱比烧碱价格低得多,采用纯碱路线既合理又经济,
故答案为:Fe(OH)3、Mn(OH)2、Mg(OH)2;纯碱;
(4)步骤⑤中反应的化学方程式为MgCO3+H2O
| ||
| ||
(5)在实验室中完成步骤⑥,则沉淀物在坩埚中加热,故答案为:坩埚.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目