��Ŀ����
����Ŀ����1����һ��������N2��H2��Ӧ����NH3����ش�
������Ӧ���������ΪE1���������������ΪE2����E1��E2����÷�ӦΪ________(����ȡ����ȡ�)��Ӧ��
����֪��1molH��H����1molN��H����1molN��N���ֱ���Ҫ��������436kJ��391kJ��946kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ___________________________________________��
��2��ʵ������50mL0.50mol��L��1������50mLijŨ�ȵ�NaOH��Һ����ͼ��ʾװ���з�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ���װ�����������ԵĴ�������һ����ȱ��һ�ֲ���������������������Ϊ___________________________��ʵ�����ṩ��0.50mol��L��1��0.55mol��L��1����Ũ�ȵ�NaOH��Һ��Ӧѡ��___________mol��L��1��NaOH��Һ����ʵ�顣

��3������������CO2���ڻ��ۣ���в����̬����������������ܵ�ȫ�����ע����ҵ�ϳ��ø�Ũ�ȵ�K2CO3��Һ����CO2������ҺX�������õ�ⷨʹK2CO3��Һ��������װ��ʾ��ͼ���£�
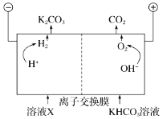
���������������ķ�Ӧ����__________________________________��H����HCO===H2O��CO2����
�ڼ���CO![]() ��������������ԭ����____________________________________��
��������������ԭ����____________________________________��
��4�������£���NaOH��Һ����SO2�õ�pH��9��Na2SO3��Һ���Լ�����Һ��![]() ��_______����������H2SO3�ĵ���ƽ�ⳣ��Ka1��1.0��10��2��Ka2��6.0��10��8��
��_______����������H2SO3�ĵ���ƽ�ⳣ��Ka1��1.0��10��2��Ka2��6.0��10��8��
���𰸡� ���� N2(g)��3H2(g)![]() 2NH3(g)����H����92kJ��mol��1 ���β�������� 0.55 4OH����4e��===2H2O��O2�� HCO���ڵ���ƽ�⣺HCO
2NH3(g)����H����92kJ��mol��1 ���β�������� 0.55 4OH����4e��===2H2O��O2�� HCO���ڵ���ƽ�⣺HCO![]() H����CO
H����CO![]() ������H���ŵ�Ũ�ȼ�Сƽ�����ƣ�CO
������H���ŵ�Ũ�ȼ�Сƽ�����ƣ�CO![]() ����(������H���ŵ�OH��Ũ������OH����HCO��Ӧ����CO
����(������H���ŵ�OH��Ũ������OH����HCO��Ӧ����CO![]() ��CO
��CO![]() ����) 60
����) 60
�������� (1)����Ӧ��������������������������Ϊ���ȷ�Ӧ��
����ѧ��Ӧ������ѧ�����������������γ��»�ѧ���ų����������ݷ���ʽ����ֱ����պͷų����������Դ˼��㷴Ӧ�Ȳ��ж����Ȼ��Ƿ�����
(2)�������ȼƵĹ������жϸ�װ�õ�ȱ��������Ϊ��ʹ��Ӧ���,NaOHӦ������
��3�������������������ӷŵ�����������
��̼��������ӳ̶ȵ���ƽ�⡢���������Ӻ�̼��������ӷ�Ӧ����̼���������
��4������Ka2=![]() ������Һ��
������Һ��![]() =
=![]() ���Դ˽����
���Դ˽����
���:(1)�ٷ�Ӧ���������ΪE1���������������ΪE2����E1>E2����÷�ӦΪ���ȷ�Ӧ��
��ˣ�������ȷ������������
���ڷ�ӦN2+3H22NH3��������3molH��H����1molN��N�����յ�����Ϊ:3��436 kJ+946 kJ=2254 kJ������2mol NH3�����γ�6mol1molN��H�����ų�������Ϊ:6��391kJ=2346kJ�����յ�������,�ų���������,�÷�ӦΪ���ȷ�Ӧ,�ų�������Ϊ��2346kJ -2254 kJ =92kJ��
��ˣ�������ȷ������N2(g)��3H2(g)![]() 2NH3(g)����H����92kJ��mol��1 ��
2NH3(g)����H����92kJ��mol��1 ��
(2)�������ȼƵĹ������֪����װ�õ�ȱ�������ǻ��β����������ʵ�����ṩ��0.50mol��L��1��0.55mol��L��1����Ũ�ȵ�NaOH��Һ��Ϊ��ʹ��Ӧ���,NaOHӦ����,����ѡ��0.55mol��L��1����Һ����ʵ����
��ˣ�������ȷ���������β����������0.55��
(3) �����������������ӷŵ�����������ˮ,�缫��ӦʽΪ4OH����4e��===2H2O��O2����
��ˣ�������ȷ������4OH����4e��===2H2O��O2����
��HCO���ڵ���ƽ�⣺HCO![]() H����CO
H����CO![]() ������H���ŵ�Ũ�ȼ�Сƽ�����ƣ�CO
������H���ŵ�Ũ�ȼ�Сƽ�����ƣ�CO![]() ����������H���ŵ�OH��Ũ������OH����HCO��Ӧ����CO
����������H���ŵ�OH��Ũ������OH����HCO��Ӧ����CO![]() ��CO
��CO![]() ������
������
��ˣ�������ȷ������HCO���ڵ���ƽ�⣺HCO![]() H����CO
H����CO![]() ������H���ŵ�Ũ�ȼ�Сƽ�����ƣ�CO
������H���ŵ�Ũ�ȼ�Сƽ�����ƣ�CO![]() ����(������H���ŵ�OH��Ũ������OH����HCO��Ӧ����CO
����(������H���ŵ�OH��Ũ������OH����HCO��Ӧ����CO![]() ��CO
��CO![]() ����)��
����)��
��4��pH=9����Һ��c��H+��=10-9mol/L������Ka2=![]() ������Һ��
������Һ��![]() =
=![]() ��=
��=![]() =60��
=60��
�ʴ�Ϊ��60��

 ��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�����Ŀ�����̿�(��Ҫ�ɷ�ΪMnO2)�������Ʊ��̼��仯����ִ�ұ�������̵Ĺ�����������ͼ��ʾ������������������һ������

�±�Ϊt��ʱ���й����ʵ�Ksp
���� | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
Ksp | 4.0��10-38 | 2.2 | 5.5 | 1.9 | 6.3 | 9.1 | 2.5 | 2.2 |
���̿�ԭ�����ķ�ӦΪ��12MnO2��C6H12O6��12H2SO4===12MnSO4��6CO2����18H2O
��1��д��һ�������ԭ�������ʵĴ�ʩ��_________________________
��2������pH ���������ɵij���Ϊ________������MnF2����ҪĿ���dz�ȥ__________ (�Ca2��������Fe3������Cu2����)
��3����Ũ�ȵģ�NH4)2S�루N4)2SO4 ��Һ�У�NH4����Ũ�ȴ�СΪ��ǰ��________���ߣ������������ �� ��=�� )��
��4����MnSO4��ȡMnCO3��MnSO4��Һ�м���(NH4)2CO3��Һ����MnCO3��ͬʱ�������Mn(OH)2�����ܵ�ԭ���У�MnCO3(s)��2OH��(aq)![]() Mn(OH)2(s)��CO
Mn(OH)2(s)��CO![]() (aq)��t��ʱ������÷�Ӧ��ƽ�ⳣ��K��_________________(����һλС��)��
(aq)��t��ʱ������÷�Ӧ��ƽ�ⳣ��K��_________________(����һλС��)��

