题目内容
【题目】碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
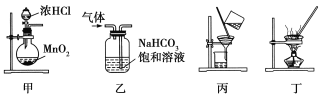
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为____________。
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中![]() 为:_____________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
为:_____________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)已知反应2HI(g) ===H2(g) + I2(g)的ΔH= +11kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为______________kJ。
(4)Bodensteins研究了下列反应:
2HI(g)![]() H2(g) + I2(g)
H2(g) + I2(g)
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
① 根据上述实验结果,该反应的平衡常数K的计算式为:___________。
② 上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数,则k逆为________(以K和k正表示)。若k正 = 0.0027min-1,在t=40min时,v正=__________min-1
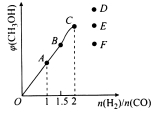
③ 由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为_________________(填字母)

【答案】(1)MnSO4;
(2)4.7×10-7;
(3)299
(4)①![]() ;②k逆= k正/K ;1.95×10-3;③ A、E
;②k逆= k正/K ;1.95×10-3;③ A、E
【解析】(1)问中根据氧化还原反应方程式来判断还原产物是中学常规考法,迁移实验室制氯气的原理可得MnSO4。
(2)体系中既有氯化银又有碘化银时,存在沉淀转化平衡:AgI(s) +Cl-![]() AgCl(s) +I-。
AgCl(s) +I-。
![]()
分子、分母同时乘以![]() ,有:
,有:![]() ,将Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17代入得:
,将Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17代入得:![]() 。
。
(3)键能一般取正值来运算,ΔH=E(反应物键能总和)-E(生成物键能总和);设1molHI(g)分子中化学键断裂时需吸收的能量为xkJ,代入计算:+11=2x-(436+151)
x =299
(4)①问中的反应是比较特殊的,反应前后气体体积相等,不同的起始态很容易达到等效的平衡状态。大家注意表格中的两列数据是正向和逆向的两组数据。
716K时,取第一行数据计算:2HI(g)![]() H2(g)+I2(g)
H2(g)+I2(g)
n(始)(取1mol) 1 0 0
Δn (0.216) (0.108) (0.108)
n(平) 0.784 (0.108) (0.108)
化学平衡常数为![]()
本小题易错点:计算式会被误以为是表达式。
②问的要点是:平衡状态下,v正= v逆,故有:k正·x2(HI) = k逆·x(H2)·x(I2)
变形:k正/ k逆={ x(H2)·x(I2)}/ x2(HI)=K
故有: k逆= k正/K
③ 问看似很难,其实注意到升温的两个效应(加快化学反应速率、使平衡移动)即可突破:先看图像右半区的正反应,速率加快,坐标点会上移;平衡(题中已知正反应吸热)向右移动,坐标点会左移。综前所述,找出A点。同理可找出E点。

【题目】已知硫铁矿的主要成分是FeS2(铁元素呈+2价,硫元素呈—1价)。以下是分析硫铁矿中FeS2含量的三种方法,各方法的操作流程图如下:
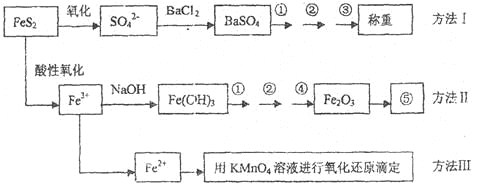
请同答下列问题:
(1)流程图中操作①、②、③分别指的是:①____________、②___________、③________。
操作④、⑤用到的主要仪器是:④_________、⑤__________(每空填1~2个仪器)。
(2)判断溶液中SO42-离子己沉淀完全的方法是______________________________________。
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,需要准确配制KMnO4标准溶液,下列因素导致所配制的溶液浓度偏大的有
A.砝码生锈 | B.定容时俯视 |
C.称量时物质和砝码位置反了(需要游码) | D.容量瓶用待装液润 |
(4)某同学采用方法Ⅱ分析矿石中的Fe含量,发现测定结果总是偏高,则产生误差的可能原因是______________________________________。
(5)称取矿石试样1.60g,按方法Ⅰ分析,称得BaSO4的质量为4.66g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是_________________________。