题目内容
如图所示,室温下向盛有3.0mLNO的试管中缓缓通入1.5mLO2(所有气体均在标准状况下测定)。
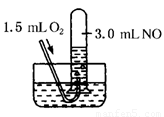
试回答下列问题:
(1)写出观察到的现象(可不写满,也可补充):
①___________________________________________________;
②___________________________________________________;
③___________________________________________________。
(2)最终试管中剩余的气体是________,体积为______。
【答案】
(1)①通入O2,试管内气体变为红棕色 ②试管内液面升高 ③最后试管内剩余无色气体
(2)NO 1.0mL
【解析】 (1)通入的O2与NO发生反应:①2NO+O2===2NO2,所以看到有红棕色气体生成。生成的NO2溶于水:②3NO2+H2O===2HNO3+NO,①②两反应的总反应为:③4NO+3O2+2H2O===4HNO3。气体消耗,又会看到液面上升。V(NO) :V(O2)≠4:3,故最后有气体剩余,不论剩余NO还是O2,均为无色气体。
(2)设1.5mLO2全部参加反应由(1)中③知:反应的NO为:
V(NO)=V(O2)×4/3=1.5mL×4/3=2.0mL,由NO总体积为3.0mL可得剩余NO气体1.0mL。

练习册系列答案
相关题目
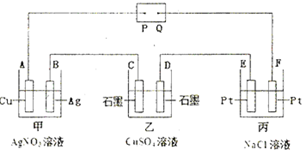
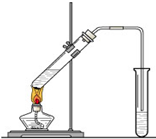 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: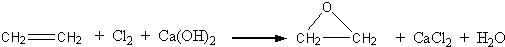
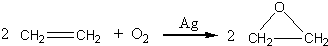
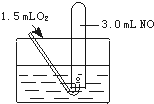 如图所示,室温下向盛有3.0mL NO的试管中缓缓通入1.5mL O2(所有气体体积均在标准状下测定).
如图所示,室温下向盛有3.0mL NO的试管中缓缓通入1.5mL O2(所有气体体积均在标准状下测定).