题目内容
制取水煤气的反应为C(s)+H2O(g)  CO(g)+H2(g) ΔH>0;在一定条件下达化学平衡后,在时间为t时突然改变条件,反应速率的变化如图所示,在t时所改变的条件是
CO(g)+H2(g) ΔH>0;在一定条件下达化学平衡后,在时间为t时突然改变条件,反应速率的变化如图所示,在t时所改变的条件是
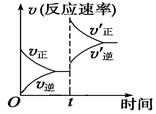
 CO(g)+H2(g) ΔH>0;在一定条件下达化学平衡后,在时间为t时突然改变条件,反应速率的变化如图所示,在t时所改变的条件是
CO(g)+H2(g) ΔH>0;在一定条件下达化学平衡后,在时间为t时突然改变条件,反应速率的变化如图所示,在t时所改变的条件是
| A.加压 | B.升温 |
| C.增大水蒸气浓度 | D.增大碳的物质的量 |
B
试题分析:在t时刻V正、V逆都增大。V正增大的多,化学平衡向正反应方向移动。由于该反应的正反应是个气体体积增大的吸热反应。A.加压 化学反应速率加快,但逆反应速率增大的多,化学平衡向逆反应方向移动。错误。B.升温 正反应、逆反应的化学反应速率加快。但升高温度,由于正反应速率增大的比逆反应速率增大的多,所以化学平衡向吸热反应方向移动及向正反应方向移动。正确。C.增大水蒸气浓度在这一瞬间,正反应速率突然增大,但逆反应速率不会变化。平衡正向移动。但与图不符。错误。 D.增大碳的物质的量由于碳但是固体。改变量的多少,化学反应速率不变,化学平衡液不移动。错误。

练习册系列答案
相关题目
 2B(g)+C(g)△H>0达平衡时,要使v(正)降低,A的浓度增大,应采取的措施是( )
2B(g)+C(g)△H>0达平衡时,要使v(正)降低,A的浓度增大,应采取的措施是( )

 CH3CH2OH(g)△H <0,达到平衡时,要使反应速率加快,同时乙烯的转化率提高,应采取的措施是
CH3CH2OH(g)△H <0,达到平衡时,要使反应速率加快,同时乙烯的转化率提高,应采取的措施是