题目内容
【题目】随着工业的迅速发展,废水的种类和数量迅猛增加,对水体的污染也日趋广泛和严重,威胁人类的健康和安全.因此工业废水的处理是当代一个重要的课题.

![]() 臭氧是一种强氧化剂,在处理含氰
臭氧是一种强氧化剂,在处理含氰![]() 废水过程中由于无二次污染,而备受关注.该过程由两步反应组成:
废水过程中由于无二次污染,而备受关注.该过程由两步反应组成:![]()
总反应的化学方程式为 ______ ,该反应![]() ______ .
______ .
![]() 工业含磷废水中含大量的
工业含磷废水中含大量的![]() ,可通过投放镁盐进行除磷.
,可通过投放镁盐进行除磷.
![]() 投放的镁盐让磷酸根形成
投放的镁盐让磷酸根形成![]() 沉淀而除磷.如图1显示,沉淀过程的 pH 对废水中磷的去除率影响很大.从如图可知,最佳除磷的pH范围是 ______
沉淀而除磷.如图1显示,沉淀过程的 pH 对废水中磷的去除率影响很大.从如图可知,最佳除磷的pH范围是 ______ ![]() 当pH较高时,磷去除率下降的原因是 ______ .
当pH较高时,磷去除率下降的原因是 ______ .
![]() 若处理后的废水中
若处理后的废水中![]() 时,试计算溶液中的
时,试计算溶液中的![]() 写出计算过程,已知
写出计算过程,已知![]()
![]() 若废水中还含有大量的
若废水中还含有大量的![]() ,投放镁盐,可得到磷酸氨镁晶体
,投放镁盐,可得到磷酸氨镁晶体![]() ,可用作化肥.写出该反应的离子方程式 ______ .
,可用作化肥.写出该反应的离子方程式 ______ .
![]() 实验表明,其他条件相同时学科王,温度越高,残余磷浓度越高.已知
实验表明,其他条件相同时学科王,温度越高,残余磷浓度越高.已知![]() 时,
时,![]() 反应时间t的变化曲线如图
反应时间t的变化曲线如图![]() 若保持其他条件不变,请在坐标图中,画出
若保持其他条件不变,请在坐标图中,画出![]() 时
时![]() 反应时间t的变化曲线示意图。
反应时间t的变化曲线示意图。
【答案】![]()
![]()
![]()
![]() 与
与![]() 反应生成更难溶的
反应生成更难溶的![]()
![]()
【解析】
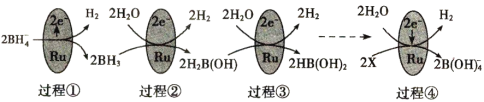
![]() 据盖斯定律,将所给的三个反应:
据盖斯定律,将所给的三个反应:![]() 可得总反应以及
可得总反应以及![]() ;
;
![]() 根据图可知,去除率较大时所对应的pH值即是;根据
根据图可知,去除率较大时所对应的pH值即是;根据![]() 与
与![]() 反应生成更难溶的
反应生成更难溶的![]() ;
;
![]() 根据
根据![]() 计算;
计算;
![]() 根据题目信息书写方程式,注意电荷守恒;
根据题目信息书写方程式,注意电荷守恒;
![]() 根据温度越高,反应速率增大,残余磷浓度越高,画出
根据温度越高,反应速率增大,残余磷浓度越高,画出![]() 时
时![]() 反应时间t的变化曲线示意图。
反应时间t的变化曲线示意图。
![]() 将所给的三个反应:
将所给的三个反应:![]() 可得总反应以及
可得总反应以及![]() ,
,![]()
故答案为:![]() ;
;![]() ;
;
![]() 从如图可知,pH在
从如图可知,pH在![]() 为除磷的最佳范围;当pH较高时,磷去除率下降的原因是
为除磷的最佳范围;当pH较高时,磷去除率下降的原因是![]() 与
与![]() 反应生成更难溶的
反应生成更难溶的![]() ;
;
故答案为:![]() ;
; ![]() 与
与![]() 反应生成更难溶的
反应生成更难溶的![]() ;
;
![]() ,即
,即![]() ,
,![]() ;
;
故答案为:![]() ;
;
![]() 废水中还含有大量的
废水中还含有大量的![]() ,投放镁盐,可得到磷酸氨镁晶体
,投放镁盐,可得到磷酸氨镁晶体![]() ,方程式为:
,方程式为:![]() ;
;
古答案为:![]() ;
;
![]() 温度越高,反应速率增大,残余磷浓度越高,则
温度越高,反应速率增大,残余磷浓度越高,则![]() 时
时![]() 反应时间t的变化曲线示意图为
反应时间t的变化曲线示意图为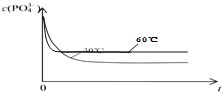 ;
;
故答案为: ;
;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案