题目内容
10.0.5molNa2CO3中( )| A. | 含3.01×1023个CO32- | B. | 该Na2CO3的质量为106g | ||
| C. | 含0.5molNa+ | D. | 含1mol氧原子 |
分析 根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$结合物质的构成计算相关物理量.
解答 解:A.N(CO32-)=0.5mol×6.02×1023/mol=3.01×1023,故A正确;
B.m(Na2CO3)=0.5mol×106g/mol=53g,故B错误;
C.由化学式可知含1molNa+,故C错误;
D.由化学式可知含1.5mol氧原子,故D错误.
故选A.
点评 本题考查物质的量的计算,为高频考点,侧重学生的分析、计算能力的考查,注意把握相关计算公式的运用以及物质的构成,难度不大.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
1.下列有关化学用语表示正确的是( )
| A. | 二氧化硅的分子式:SiO2 | |
| B. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{78}$I | |
| C. | 甲基的电子式: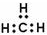 | |
| D. | 硫酸钠的电离方程式:Na2SO4═2Na++SO${\;}_{4}^{2-}$ |
18.提纯含有少量Ba(NO3)2杂质的KNO3溶液,可使用的方法为( )
| A. | 加入过量Na2CO3溶液、过滤、除去沉淀,溶液中补加适量硝酸 | |
| B. | 加入过量K2SO4溶液、过滤、除去沉淀,溶液中补加适量硝酸 | |
| C. | 加入过量K2CO3溶液、过滤、除去沉淀,溶液中补加适量盐酸 | |
| D. | 加入过量K2CO3溶液、过滤、除去沉淀,溶液中补加适量硝酸 |
5.以下操作或实验装置不能用于分离物质的是( )
| A. | 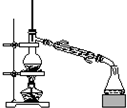 | B. |  | C. | 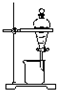 | D. | 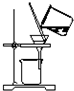 |
15.某化学兴趣小组利用下列试剂:铁粉、锌粉、0.1mol•L-l FeCl3溶液,0.1mol•L-l FeCl2溶液、KSCN溶液、新制氯水,探究Fe2+、Fe3+的氧化性、还原性,并利用实验结论解决一些问题.
(1)用所给试剂写出体现Fe2+具有还原性的反应的化学方程式:2FeCl2+Cl2═2FeCl3.
(2)设计实验方案,完成下列表格.
(3)该兴趣小组为说明“Fe2+具有氧化性”,提出了向FeCl2溶液中加入锌粉,观察实验现象的方案,该反应的离子方程式为Fe2++Zn═Zn2++Fe.
(4)某反应中反应物与生成物有Fe3+、Mn2+、H+、MnO4-、H2O和一种未知离子X.
①已知MnO4-在反应中得到电子,则X是Fe2+.
②该反应的离子方程式是MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O.
(1)用所给试剂写出体现Fe2+具有还原性的反应的化学方程式:2FeCl2+Cl2═2FeCl3.
(2)设计实验方案,完成下列表格.
| 探究内容 | 实验方案 | 实验现象 |
| 探究Fe3+具有氧化性 | 取少量0.1mol/L FeCl3溶液,往溶液中加入足量铁粉,再加入少量KSCN溶液. | 加入铁粉后,溶液颜色变为浅绿色_.加入KSCN溶液后,溶液不变色. |
(4)某反应中反应物与生成物有Fe3+、Mn2+、H+、MnO4-、H2O和一种未知离子X.
①已知MnO4-在反应中得到电子,则X是Fe2+.
②该反应的离子方程式是MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O.
10.磷酸(H3PO4)在水中可分三步电离,能够以H3PO4、H2PO4-、HPO42-、PO43-等四种粒子形式存在,当溶液的pH发生变化时,其中任一粒子的物质的量占四种粒子总物质的量的分数δ(分数分布)也可能发生变化.图1是某浓度H3PO4溶液中各种粒子的物质的量分数δ随pH的变化曲线.用NaOH标准溶液滴定该H3PO4溶液,绘得滴定曲线如图2.下列说法不正确的是( )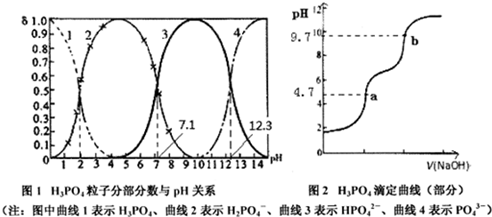

| A. | 从图1可知H3PO4、HPO42-、PO43-不能大量共存,0.01mol•L-1NaH2PO4溶液中c(H2PO4-)>c(H3PO4)>c(HPO42-) | |
| B. | PO43-+H2O?0H-+HPO42-的平衡常数为10-1.7 | |
| C. | 从a点到b点的反应为H2PO4-+OH-=HPO42-+H2O,可以选用pH计确定滴定终点,无需添加指示剂 | |
| D. | 在Na2HPO4溶液中存在c(Na+)+c(OH-)=c(H+)+c(PO43-)+2c(HPO42-)+3c(H2PO4-)+4c(H3PO4) |
11.下面四种变化中,有一种变化与其他三种变化类型不同的是:( )
| A. | CH3CH2OH+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O | |
| B. | CH3CH2Br+KOH$→_{△}^{乙醇}$CH2=CH2↑+KBr+H2O | |
| C. | 2 CH3CH2OH$→_{140℃}^{浓H_{2}SO_{4}}$CH3CH2OCH2CH3+H2O | |
| D. | CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O |
 目前半导体生产展开了一场“铜芯片”革命--在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:
目前半导体生产展开了一场“铜芯片”革命--在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下: