题目内容
1.下列有关化学用语表示正确的是( )| A. | 二氧化硅的分子式:SiO2 | |
| B. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{78}$I | |
| C. | 甲基的电子式: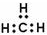 | |
| D. | 硫酸钠的电离方程式:Na2SO4═2Na++SO${\;}_{4}^{2-}$ |
分析 A.二氧化硅为原子晶体;
B.元素符号左上角为质量数;
C.甲基中碳原子最外层为7个电子;
D.硫酸钠为强电解质,完全电离生成钠离子和硫酸根离子.
解答 解:A.二氧化硅为原子晶体,不存在分子,故A错误;
B.质子数为53,中子数为78的碘原子,质量数为53+78=131,表示为:53131I,故B错误;
C.甲基中碳原子最外层为7个电子,甲基的电子式为 ,故C错误;
,故C错误;
D.硫酸钠为强电解质,完全电离生成钠离子和硫酸根离子,硫酸钠的电离方程式:Na2SO4═2Na++SO42-,故D正确;
故选:D.
点评 本题考查了化学用语的使用,明确电子式、原子符号表示方法是解题关键,注意只有分子晶体才存在分子,题目难度不大.

练习册系列答案
相关题目
11.NaHCO3和Na2O2按2:1的个数之比混合,在密闭容器中加热使之充分反应,然后趁热排出气体物质,容器内残留物的成分是( )
| A. | Na2O2和NaHCO3 | B. | NaHCO3和Na2CO3 | C. | NaOH和Na2CO3 | D. | 只有Na2CO3 |
9.有机物E的名称是( )
| A. | 丁烷 | B. | 2-甲基丙烷 | C. | 1-甲基丙烷 | D. | 甲烷 |
6.下列关于金属的保护的说法中正确的是( )
| A. | 以铝为阴极极,可以在铝表面生成一层致密的氧化膜 | |
| B. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 | |
| C. | 生铁(铁碳合金)比纯铁耐酸能力更强 | |
| D. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
13.下列离子方程式正确的是( )
| A. | 过量的SO2通入氨水中:SO2+2NH3•H2O═2 NH4++SO32-+H2O | |
| B. | SO2通入溴水中:Br2+SO2+2H2O═2H++SO42-+2HBr | |
| C. | 少量SO2通入漂白粉溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| D. | 酸雨久置pH变小:2H2SO3+O2═4H++2 SO42- |
10.0.5molNa2CO3中( )
| A. | 含3.01×1023个CO32- | B. | 该Na2CO3的质量为106g | ||
| C. | 含0.5molNa+ | D. | 含1mol氧原子 |
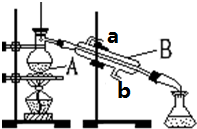 蒸馏是净化水的方法之一,如图是实验室常用的蒸馏装置,回答下列问题:
蒸馏是净化水的方法之一,如图是实验室常用的蒸馏装置,回答下列问题: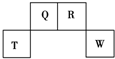 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中,T所处的周期序数与主族序数相等.请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中,T所处的周期序数与主族序数相等.请回答下列问题: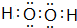 ,存在的化学键类型有非极性键和极性键.
,存在的化学键类型有非极性键和极性键.