题目内容
【题目】常温下,浓度均为1.0 mol·L-1的NH3·H2O和NH4Cl混合溶液10 mL,测得其pH为9.3。下列有关叙述正确的是( )
A.加入适量的NaCl,可使c(NH![]() )=c(Cl-)
)=c(Cl-)
B.滴加几滴浓氨水,c(NH![]() )减小
)减小
C.滴加几滴浓盐酸,![]() 的值减小
的值减小
D.1.0 mol·L-1的NH4Cl溶液中c(NH![]() )比该混合溶液中的大
)比该混合溶液中的大
【答案】A
【解析】选A。根据题意等浓度的两种溶液混合后,溶液呈碱性,说明NH3·H2O的电离程度大于NH4Cl的水解程度,即c(NH![]() )>c(Cl-),加入适量的NaCl,可使c(NH
)>c(Cl-),加入适量的NaCl,可使c(NH![]() )=c(Cl-),A项正确;滴加几滴浓氨水,虽然电离程度减小,但c(NH
)=c(Cl-),A项正确;滴加几滴浓氨水,虽然电离程度减小,但c(NH![]() )仍增大,B项错误;加入几滴浓盐酸后,c(OH-)减小,由于电离常数不变,
)仍增大,B项错误;加入几滴浓盐酸后,c(OH-)减小,由于电离常数不变,![]() 的值增大,C项错误;由于NH3·H2O的存在抑制了NH
的值增大,C项错误;由于NH3·H2O的存在抑制了NH![]() 的水解,1.0 mol·L-1的NH4Cl溶液中c(NH
的水解,1.0 mol·L-1的NH4Cl溶液中c(NH![]() )比该混合溶液中的小,D项错误。
)比该混合溶液中的小,D项错误。

【题目】为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后,在向滤液中加入适量的盐酸,这种试剂是
A. NH3·H2O B. NaOH C. Na2CO3 D. MgCO3
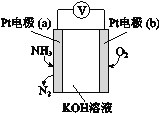
【题目】在2L恒容密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
 (1)写出该反应的平衡常数表达式:K= 。
(1)写出该反应的平衡常数表达式:K= 。
已知:![]() >
>![]() ,则该反应是 热反应。
,则该反应是 热反应。
(2)图中表示NO2浓度的变化的曲线是 。
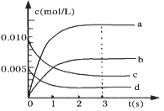
用O2表示从0—2s内该反应的平均速率υ(O2)= 。
(3)能说明该反应已达到平衡状态的是 。
a.C(NO2)=2C(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4) 为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂