题目内容
【题目】在2L恒容密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
 (1)写出该反应的平衡常数表达式:K= 。
(1)写出该反应的平衡常数表达式:K= 。
已知:![]() >
>![]() ,则该反应是 热反应。
,则该反应是 热反应。
(2)图中表示NO2浓度的变化的曲线是 。
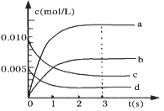
用O2表示从0—2s内该反应的平均速率υ(O2)= 。
(3)能说明该反应已达到平衡状态的是 。
a.C(NO2)=2C(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4) 为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
【答案】(1)K= ,放热
,放热
(2)b,1.5×10-3mol·L-1·s-1
(3)b、c(4)c
【解析】
试题分析:(1)写出该反应的平衡常数表达式:K= ;
;![]() >
>![]() ,温度越高K越大,说明升高温度平衡正向移动,则该反应是吸热热反应;(2)NO2是产物,随反应进行浓度增大,平衡时c(NO2)为NO浓度的变化量△c(NO),由表中数据可知3s时反应达平衡,平衡时n(NO)=0.007mol,△n(NO)=0.02mol-0.007mol=0.013mol,c(NO2)=
,温度越高K越大,说明升高温度平衡正向移动,则该反应是吸热热反应;(2)NO2是产物,随反应进行浓度增大,平衡时c(NO2)为NO浓度的变化量△c(NO),由表中数据可知3s时反应达平衡,平衡时n(NO)=0.007mol,△n(NO)=0.02mol-0.007mol=0.013mol,c(NO2)=![]() =0.0065mol/L;v(NO) =
=0.0065mol/L;v(NO) = ![]() =
= ![]() = 3 × 10-3mol·L-1·s-1 ,再根据速率之比等于化学计量数之比计算v(O2)=1.5×10-3mol·L-1·s-1;(3) 能说明该反应已达到平衡状态的是:a. 任意状态都有v(NO2)=2v(O2),不一定平衡;b.正反应物质的量减少,压强是变量,容器内压强保持不变一定平衡;c.正逆反应速率比等于系数比,v逆(NO)=2v正(O2)一定平衡;d.根据质量守恒,气体质量不变,
= 3 × 10-3mol·L-1·s-1 ,再根据速率之比等于化学计量数之比计算v(O2)=1.5×10-3mol·L-1·s-1;(3) 能说明该反应已达到平衡状态的是:a. 任意状态都有v(NO2)=2v(O2),不一定平衡;b.正反应物质的量减少,压强是变量,容器内压强保持不变一定平衡;c.正逆反应速率比等于系数比,v逆(NO)=2v正(O2)一定平衡;d.根据质量守恒,气体质量不变,![]() ,容器内物质的密度是恒量,密度保持不变不一定平衡;(4)及时分离除NO2气体,反应体系浓度减小,速率减慢;正反应放热,适当升高温度平衡逆向移动;增大O2的浓度,反应物浓度增大,速率加快、平衡正向移动;选择高效催化剂平衡不移动。
,容器内物质的密度是恒量,密度保持不变不一定平衡;(4)及时分离除NO2气体,反应体系浓度减小,速率减慢;正反应放热,适当升高温度平衡逆向移动;增大O2的浓度,反应物浓度增大,速率加快、平衡正向移动;选择高效催化剂平衡不移动。