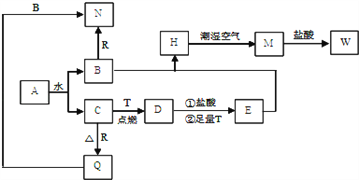
��Ŀ����
����Ŀ��SO2�Ĵ������ǹ�ҵ��ȡ����Ĺؼ�����֮һ���÷�Ӧ�Ļ�ѧ����ʽΪ��2SO2+O22SO3 �� ��H��0��
��ش��������⣺
��1���жϸ÷�Ӧ�ﵽƽ��״̬�ı�־��������ĸ����
a��SO2��SO3Ũ����� b��SO2�ٷֺ������ֲ���
c�������������ѹǿ���� d��SO3������������SO2�������������
��2�����÷�Ӧ����ƽ��״̬ʱ�����������������£����д�ʩ�����������SO2ƽ��ת���ʵ��� �� ������ĸ��
a����װ�����ٳ���N2 b����װ�����ٳ���O2
c���ı䷴Ӧ�Ĵ��� d�������¶�
��3����0.050mol SO2��g����0.030mol O2��g�������ݻ�Ϊ1L���ܱ������У���һ�������´ﵽƽ�⣬���c��SO3��=0.040mol/L������������·�Ӧ��ƽ�ⳣ��K��SO2��ת���ʣ�����д��������̣���
��ƽ�ⳣ��K=����ƽ��ʱ��SO2��ת���ʦ���SO2��=
��4��SO2β�����ñ���Na2SO3��Һ���գ�����SO2������Ⱦ���ɵõ���Ҫ�Ļ���ԭ��NaHSO3 �� ��֪NaHSO3
��Һͬʱ������������ƽ�⣺��HSO3��SO32��+H+ �� ��HSO3��+H2OH2SO3+OH���������£�0��l mol/L NaHSO3��Һ��pH��7�������Һ��c��H2SO3��c��SO32���������������=����������
���𰸡�
��1��bc
��2��bd
��3��1.6��103��80%
��4����
���������⣺��1��a��SO2��SO3Ũ����ȣ�������ô���淴Ӧ������ͬ������˵����Ӧ�ﵽƽ��״̬����a���� b��SO2�ٷֺ������ֲ�����ƽ���־����b��ȷ��
c����Ӧǰ��������������仯�������������ѹǿ����˵����Ӧ�ﵽƽ��״̬����C��ȷ��
d��SO3������������SO2����������������㷴Ӧ������У�����˵����Ӧ�ﵽƽ��״̬����d����
���Դ��ǣ�bc����2�����÷�Ӧ����ƽ��״̬ʱ�����������������£����SO2ƽ��ת���ʣ�ƽ��������У�
a����װ�����ٳ���N2 �� ���ݺ�����������ѹ�����ѹ���䣬ƽ�ⲻ�䣬��a����
b�����ַ�Ӧ������һ�ֻ������һ�ֵ�ת���ʣ���װ�����ٳ���O2 �� ����߶�������ת���ʣ���b��ȷ��
c���ı䷴Ӧ�Ĵ������ı䷴Ӧ���ʲ��ı仯ѧƽ�⣬��c����
d����Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ��������У���������ת��������d��ȷ��
���Դ��ǣ�bd�� ��3����0.050mol SO2��g����0.030mol O2��g�������ݻ�Ϊ1L���ܱ������У���һ�������´ﵽƽ�⣬���c��SO3��=0.040mol/L��
2SO2+ | O2 | 2SO3 | ||
��ʼ����mol�� | 0.05 | 0.03 | 0 | |
�仯����mol�� | 0.04 | 0.02 | 0.04 | |
ƽ������mol�� | 0.01 | 0.01 | 0.04 |
��ƽ�ⳣ��K= ![]() =1.6��103 �� ���Դ��ǣ�1.6��103��
=1.6��103 �� ���Դ��ǣ�1.6��103��
��ƽ��ʱ��SO2��ת���ʦ���SO2��= ![]() ��100%=80%�����Դ��ǣ�80%�� ��4����֪NaHSO3�е�HSO3�����ܵ�������ˮ�⣺HSO3��H++SO32�����������ԣ�HSO3��+H2OH2SO3 +OH�� ˮ���Լ��ԣ������£�0.1molL��1NaHSO3��Һ��pHС��7��
��100%=80%�����Դ��ǣ�80%�� ��4����֪NaHSO3�е�HSO3�����ܵ�������ˮ�⣺HSO3��H++SO32�����������ԣ�HSO3��+H2OH2SO3 +OH�� ˮ���Լ��ԣ������£�0.1molL��1NaHSO3��Һ��pHС��7��
˵���������ˮ�⣬�ʣ�c��SO32������c��H2SO3�������Դ��ǣ�����
�����㾫�������û�ѧƽ��״̬���ʼ������ͻ�ѧƽ��״̬���ж϶���Ŀ�����жϼ��ɵõ��𰸣���Ҫ��֪��ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч����״̬�жϣ���v(B��)=v(B��)��v(C��):v(D��)=x : y��c(C)��C%��n(C)%�Ȳ������A��B��C��DΪ���壬��m+n��x+y��ѹǿ�㶨����ϵ��ɫ�����λʱ����ij�����ڻ�ѧ���Ķ����������γ�������ϵƽ��ʽ���㶨��m+n �� x+y���ȣ�

 �������ͬ������ϵ�д�
�������ͬ������ϵ�д�����Ŀ������ѪҺ�������Ҫ�����ƽ�⣺CO2+H2OH2CO3 ![]() HCO3�� �� ʹ����ѪҺpH������7.35��7.45������ͻᷢ�����ж�����ж�����pH��c��HCO3������c��H2CO3���仯��ϵ���±���
HCO3�� �� ʹ����ѪҺpH������7.35��7.45������ͻᷢ�����ж�����ж�����pH��c��HCO3������c��H2CO3���仯��ϵ���±���
c��HCO | 1.0 | 17.8 | 20.0 | 22.4 |
pH | 6.10 | 7.35 | 7.40 | 7.45 |
����˵������ȷ���ǣ� ��
A.��������ѪҺ�У�HCO ![]() ��ˮ��̶ȴ��ڵ���̶�
��ˮ��̶ȴ��ڵ���̶�
B.����ѪҺ���ж�ʱ����ע��NaHCO3��Һ����
C.pH=7.00��ѪҺ�У�c��H2CO3����c��HCO ![]() ��
��
D.pH=7.40��ѪҺ�У�HCO ![]() ��ˮ��̶�һ������H2CO3�ĵ���̶�
��ˮ��̶�һ������H2CO3�ĵ���̶�