��Ŀ����
����Ŀ����֪AΪ����ɫ���壬T��RΪ���ֳ�������;�ܹ�Ľ������ʣ�D�Ǿ��д��Եĺ�ɫ���壬C����ɫ��ζ�����壬H�ǰ�ɫ������W��Һ�м���KSCN����Ѫ��ɫ��
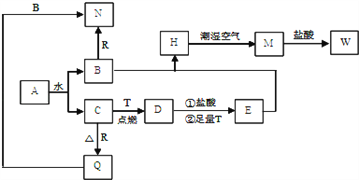
��1��д���������ʵĻ�ѧʽ��D______ N_______
��2��B��E��͵õ�H���ڳ�ʪ�����б��M�Ĺ����У����ܹ۲쵽������_______�� H�ڳ�ʪ�����б��M�Ĺ����з����Ļ�ѧ����ʽΪ��___________________��
��3����Ҫ��д����ʽ�� B��R��Ӧ����N�����ӷ���ʽ��______________________��M��W�����ӷ���ʽ��____________________��
���𰸡� Fe3O4 NaAlO2 ��Һ�г��ְ�ɫ�������ڿ�����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ 4Fe(OH)2+O2+2H2O=4Fe(OH)3 2Al+2OH��+2H2O=2 AlO2��+3H2�� Fe(OH)3+3H+ =Fe3++3H2O��
��������AΪ����ɫ����Na2O2������ˮ��Ӧ�õ�BΪNaOH��CΪO2��NaOH��Al������Ӧ��2Al+2NaOH+2H2O=2NaAlO2+3H2���õ�N��NaAlO2��O2��R��Al������Ӧ4Al+3O2![]() 2Al2O3�õ�Q Al2O3��Al2O3��NaOH��Һ������Ӧ��Al2O3+2NaOH=2NaAlO2+2H2O���õ�N��NaAlO2��O2��T��Fe�ڵ�ȼʱ��Ӧ�õ�D��Fe3O4��Fe3O4��������HCl��Fe�����µõ�E:FeCl2��FeCl2��NaOH������Ӧ�õ�H:Fe(OH)2��Fe(OH)2�ڳ�ʪ�Ŀ����з�����Ӧ4Fe(OH)2 + O2+2H2O == 4Fe(OH)3�õ�M��Fe(OH)3��Fe(OH)3��HCl��������кͷ�ӦFe(OH)3+3HCl= FeCl3+3H2O���õ�W��FeCl3��ˮ����1��DΪFe3O4��NΪNaAlO2����2��BΪNaOH����EΪFeCl2��͵õ�HΪFe(OH)2���ڳ�ʪ�����б��MΪ Fe(OH)3�Ĺ����У��۲쵽�������ǣ���Һ�г��ְ�ɫ�������ڿ�����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ��H�ڳ�ʪ�����б��M�Ĺ����з����Ļ�ѧ����ʽΪ��4Fe(OH)2+O2+2H2O=4Fe(OH)3����3��B��NaOH����R��Al����Ӧ����N��NaAlO2�������ӷ���ʽΪ2Al+2OH��+2H2O=2 AlO2��+3H2����M [Fe(OH)3]��W��FeCl3�������ӷ���ʽΪ��Fe(OH)3+3H+ =Fe3++3H2O��
2Al2O3�õ�Q Al2O3��Al2O3��NaOH��Һ������Ӧ��Al2O3+2NaOH=2NaAlO2+2H2O���õ�N��NaAlO2��O2��T��Fe�ڵ�ȼʱ��Ӧ�õ�D��Fe3O4��Fe3O4��������HCl��Fe�����µõ�E:FeCl2��FeCl2��NaOH������Ӧ�õ�H:Fe(OH)2��Fe(OH)2�ڳ�ʪ�Ŀ����з�����Ӧ4Fe(OH)2 + O2+2H2O == 4Fe(OH)3�õ�M��Fe(OH)3��Fe(OH)3��HCl��������кͷ�ӦFe(OH)3+3HCl= FeCl3+3H2O���õ�W��FeCl3��ˮ����1��DΪFe3O4��NΪNaAlO2����2��BΪNaOH����EΪFeCl2��͵õ�HΪFe(OH)2���ڳ�ʪ�����б��MΪ Fe(OH)3�Ĺ����У��۲쵽�������ǣ���Һ�г��ְ�ɫ�������ڿ�����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ��H�ڳ�ʪ�����б��M�Ĺ����з����Ļ�ѧ����ʽΪ��4Fe(OH)2+O2+2H2O=4Fe(OH)3����3��B��NaOH����R��Al����Ӧ����N��NaAlO2�������ӷ���ʽΪ2Al+2OH��+2H2O=2 AlO2��+3H2����M [Fe(OH)3]��W��FeCl3�������ӷ���ʽΪ��Fe(OH)3+3H+ =Fe3++3H2O��

 �ƸԴ��ž�ϵ�д�
�ƸԴ��ž�ϵ�д�