题目内容
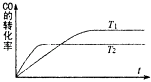
【题目】二氧化锰是化学工业中常用的氧化剂和有机合成中的催化剂,其主要制备方法是碳酸锰热分解,反应原理为2MnCO3+O2═2MnO2+2CO2 . 经研究发现该反应过程为①MnCO3═MnO+CO2 ②2MnO+O2═2MnO2 .
回答下列问题:
(1)某温度下该平衡体系的压强为P,CO2、O2的物质的量分别为n1和n2 , 用平衡分压代替平衡浓度,碳酸锰热分解反应的平衡常数K=(分压=总压×物质的量分数);K与反应①、②的平衡常数K1、K2的关系为 .
(2)反应②在低温下能自发进行,则其△H0(填“>”、“<”或“=”).
【答案】
(1)![]() ;K=K12×K2
;K=K12×K2
(2)<
【解析】解:(1)反应①的平衡常数表达式K1= ![]() =
= 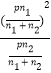 =
= ![]() ,K与反应①、②的平衡常数K1、K2关系为:2MnCO3+O2═2MnO2+2CO2为方程①的系扩大2倍后与②之和所以K=K12×K2 , 所以答案是:
,K与反应①、②的平衡常数K1、K2关系为:2MnCO3+O2═2MnO2+2CO2为方程①的系扩大2倍后与②之和所以K=K12×K2 , 所以答案是: ![]() ;K=K12×K2;(2)反应②在低温下能,只有△H<0,△G<0反应自发,
;K=K12×K2;(2)反应②在低温下能,只有△H<0,△G<0反应自发,
所以答案是:<.
【考点精析】本题主要考查了化学平衡的计算的相关知识点,需要掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%才能正确解答此题.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案
相关题目