��Ŀ����
3��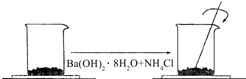 ��һ��С�ձ������ 40g Ba��OH��2•8H2O��ĩ����С�ձ����������ѵ���4��5��ˮ�IJ���Ƭ�ϣ�Ȼ�����20g NH4Cl���壬���ò�����Ѹ�ٽ��裮��ͼ��ʾ���ش��������⣺
��һ��С�ձ������ 40g Ba��OH��2•8H2O��ĩ����С�ձ����������ѵ���4��5��ˮ�IJ���Ƭ�ϣ�Ȼ�����20g NH4Cl���壬���ò�����Ѹ�ٽ��裮��ͼ��ʾ���ش��������⣺��1���˷�Ӧ�Ļ�ѧ����ʽ��Ba��OH��2•8H2O+2NH4Cl=BaCl2+2NH3��+10H2O��
��2��ʵ����Ҫ�ò�����Ѹ�ٽ����ԭ���ǽ���ʹ������ֽӴ������ٷ�Ӧ��
��3����Ӧ�����ʺ�״��ԭ���Ƿ�Ӧ��������ˮ���ɣ�
��4���÷�ӦΪ���ȷ�Ӧ���������ڷ�Ӧ���������С����������������������С���ȡ�����
���� ��1���Ȼ�狀����������ķ�Ӧ���ɰ�����ˮ�Լ��Ȼ�����
��2����������ķ�Ӧ�ò��������������ڳ�ֽӴ������ٷ�Ӧ���У�
��3���Ȼ����κ�ǿ�����������ķ�Ӧ���ɰ�����ˮ�Լ��Ȼ������Դ˽��ͷ�Ӧ����
��4������Ƭ�Ͻ������С�ձ�ճ��һ��˵�������������Ȼ�淋ķ�Ӧ�����ȷ�Ӧ����Ӧ���������С�����������������
��� �⣺��1���Ȼ��������Σ��ܺ�ǿ������������Ӧ���ɰ�����ˮ�Լ��Ȼ���������ʽΪ��Ba��OH��2•8H2O+2NH4Cl=BaCl2+2NH3��+10H2O��
�ʴ�Ϊ��Ba��OH��2•8H2O+2NH4Cl=BaCl2+2NH3��+10H2O��
��2���ò�����Ѹ�ٽ��裬����֪���������������ǽ���ʹ������ֽӴ�����Ӧ��
�ʴ�Ϊ������ʹ������ֽӴ������ٷ�Ӧ��
��3����Ӧ�����ɺ�״��ԭ���Ƿ�Ӧ����������ˮ��Ե�ʣ�
�ʴ�Ϊ����Ӧ��������ˮ���ɣ�
��4������Ƭ�Ͻ������С�ձ�ճ��һ��˵�������������Ȼ�淋ķ�Ӧ�����ȷ�Ӧ������Ӧ���������С�����������������
�ʴ�Ϊ������С�ڣ�
���� ���⿼�����ȷ�Ӧ��̽����������Ŀ�ѶȲ���ע������Ȼ�狀�����������Ӧ��ԭ������Ӧ����ע��ӷ�Ӧ�����������������Ĺ�ϵ������

 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�| A�� | ת��ʱ��Ҫ�ò��������� | |
| B�� | ������ƽ��ȡ58.50��ʳ�Σ���ˮ���Ƴ�1����Һ��NaCl��ҺŨ��Ϊ1mol•L-1 | |
| C�� | �ܽ�ʳ�ε��ձ�Ҫϴ��2��3�β���ϴ��Һת�Ƶ�����ƿ�� | |
| D�� | ����ɼ����ܽ� |
| Ԫ�ش��� | X | Y | Z | W |
| ԭ�Ӱ뾶/pm | 160 | 143 | 70 | 66 |
| ��Ҫ���ϼ� | +2 | +3 | +5+3-3 | -2 |
| A�� | X��YԪ�صĽ����ԣ�X��Y | |
| B�� | һ�������£�Z������W�ij�������ֱ������ZW2 | |
| C�� | Y������������ˮ����������ϡ��ˮ | |
| D�� | Z������������ˮ������ǿ�� |

| A�� | ��ϵͳ��ֻ����3����ʽ������ת�� | |
| B�� | װ��X��Y�γɵ���ϵͳ��ʵ�����ʵ����ŷţ�����ʵ�ֻ�ѧ������ܼ����ȫת�� | |
| C�� | װ��Y�и����ĵ缫��ӦʽΪ��O2+2H2O+4e-�T4OH- | |
| D�� | װ��X��ʵ��ȼ�ϵ�ص�ȼ������ |
| A�� | SO2ͨ��ʯ����Һ�У���Һ��� | |
| B�� | ���������ˮ������Ӧʱ��������� | |
| C�� | ��һ����������Һ����������Һ��Ͼ��ã��۲췢����Һ��ɫ�������� | |
| D�� | ������CuSO4���������ˮ�Ҵ��У����ã��ϲ���Һ��ΪCuSO4���� |