题目内容
15.下列有关实验表述错误的是( )| A. | SO2通入石蕊溶液中,溶液变红 | |
| B. | 铁粉与高温水蒸气反应时,固体逐渐变黑 | |
| C. | 将一定量草酸溶液与高锰酸钾溶液混合静置,观察发现溶液褪色速率逐渐变慢 | |
| D. | 将少量CuSO4固体加入无水乙醇中,振荡后静置,上层清液即为CuSO4胶体 |
分析 A.二氧化硫和水反应生成亚硫酸而使其水溶液呈酸性,酸能使酸碱指示剂变色;
B.高温下,铁和水蒸气反应生成四氧化三铁和氢气;
C.反应速率与浓度成正比;
D.硫酸铜在乙醇中的溶解度较小,能形成胶体.
解答 解:A.二氧化硫和水反应生成亚硫酸而使其水溶液呈酸性,酸能使酸碱指示剂变色,所以SO2通入石蕊溶液中,溶液变红,故A正确;
B.高温下,铁和水蒸气反应生成四氧化三铁和氢气,Fe和四氧化三铁都是黑色固体,故B错误;
C.反应速率与浓度成正比,随着反应的进行,反应物浓度降低,则反应速率减小,所以观察发现溶液褪色速率逐渐变慢,故C正确;
D.硫酸铜在乙醇中的溶解度较小,能形成胶体,所以将少量CuSO4固体加入无水乙醇中,振荡后静置,上层清液即为CuSO4胶体,故D正确;
故选B.
点评 本题考查元素化合物知识,为高频考点,侧重考查二氧化硫、铁、反应速率影响因素、胶体等知识点,注意:二氧化硫能使品红溶液褪色,但不能使酸碱指示剂褪色,为易错点.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
10.以下有关物质结构的描述正确的是( )
①甲苯分子中的所有原子可能共平面
②苯乙烯分子中的所有原子可能共平面
③二氯甲烷分子为正四面体结构
④乙烷分子中的所有原子不可能都在同一平面内.
①甲苯分子中的所有原子可能共平面
②苯乙烯分子中的所有原子可能共平面
③二氯甲烷分子为正四面体结构
④乙烷分子中的所有原子不可能都在同一平面内.
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
20.在一恒定容积的容器中充入4mol A和2mol B发生如下反应:2A(g)+B(g)?ξΧ(γ),达到平衡后,Χ的体积分数为Ω%,若维持容积和温度不变,按1.2μολΑ、0.6μολΒ和2.8μολΧ为起始物质,达到平衡后,Χ的体积分数仍为Ω%,则ξ的<为( )
| A. | 只能为2 | B. | 只能为3 | ||
| C. | 可能为2,也可能为3 | D. | 无法确定 |
7.设NA为阿伏加德罗常数的数值.下列说法正确的是( )
| A. | 标准状况下,22.4L由NO2和NO组成的混合气体中含有的氧原子数目为2NA | |
| B. | 常温常压下,含34gH2O2的溶液中氢原子的物质的量为2moI | |
| C. | 高温下,16.8gFe与足量水蒸气完全反应,失去0.8NA个电子 | |
| D. | 常温下,100mLlmol.L-l盐酸与4.6 g钠反应生成0.05 molH2 |
 固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ;某科学实验将6mol CO2和8mol H2充入一容积为2L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后的数字表示对应的坐标):回答下列问题:
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ;某科学实验将6mol CO2和8mol H2充入一容积为2L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后的数字表示对应的坐标):回答下列问题: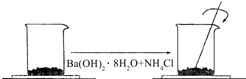 在一个小烧杯里,加入 40g Ba(OH)2•8H2O粉末,将小烧杯放在事先已滴有4~5滴水的玻璃片上.然后加入20g NH4Cl晶体,并用玻璃棒迅速搅拌.如图所示.回答下列问题:
在一个小烧杯里,加入 40g Ba(OH)2•8H2O粉末,将小烧杯放在事先已滴有4~5滴水的玻璃片上.然后加入20g NH4Cl晶体,并用玻璃棒迅速搅拌.如图所示.回答下列问题: