题目内容
【题目】实施以节约能源和减少废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。试运用所学知识,回答下列问题:
(1)已知在一定温度下,①C(s)+CO2(g) ![]() 2CO(g) △H1=a kJ/mol 平衡常数K1;
2CO(g) △H1=a kJ/mol 平衡常数K1;
②CO(g)+H2O(g) ![]() H2(g)+CO2(g) △H2=b kJ/mol 平衡常数K2;
H2(g)+CO2(g) △H2=b kJ/mol 平衡常数K2;
某反应的平衡常数表达式K3=![]() ,请写出此反应的热化学方程式:__________,K1、K2、K3之间的关系是:_____________。
,请写出此反应的热化学方程式:__________,K1、K2、K3之间的关系是:_____________。
(2)将原料气按n(CO2):n(H2)=1:4置于密闭容器中发生CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g)反应,测得H2O(g)的物质的量分数与温度的关系如图所示
CH4(g)+2H2O(g)反应,测得H2O(g)的物质的量分数与温度的关系如图所示
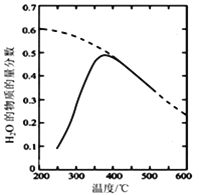 (虚线表示平衡曲线)。
(虚线表示平衡曲线)。
①该反应的平衡常数K随温度降低而________(填“增大”或“减小”)。
②在密闭恒温(高于100℃)恒容装置中进行该反应,下列能说明达到平衡状态的是_____。
A.混合气体密度不再改变
B.混合气体压强不再改变
C.混合气体平均摩尔质量不再改变
D. n(CO2):n(H2)=1:2
③200℃达到平衡时体系的总压强为p,该反应平衡常数Kp的计算表达式为______。(不必化简,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(3)500℃时,CO与水反应生成CO2和H2。将CO2和H2分离得到H2的过程示意图如下。
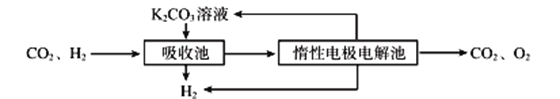
①吸收池中所有离子浓度的等式关系是____________________________。
②结合电极反应式,简述K2CO3溶液的再生原理:___________________。
【答案】 K3= K1·K2 C(s)+H2O(g) ![]() CO(g)+H2(g) △H= (a+b) kJ/mol 增大 BC
CO(g)+H2(g) △H= (a+b) kJ/mol 增大 BC ![]() c(K+) + c(H+) == 2c(CO32-) + c(HCO3-) + c(OH-) 阴极反应:2H2O+2e-=H2↑+2OH-,OH-+HCO3-=CO32-+H2O,使K2CO3溶液得以再生。
c(K+) + c(H+) == 2c(CO32-) + c(HCO3-) + c(OH-) 阴极反应:2H2O+2e-=H2↑+2OH-,OH-+HCO3-=CO32-+H2O,使K2CO3溶液得以再生。
【解析】平衡常数为生成物的浓度幂之积除以反应物的浓度幂之积,平衡常数中,分子为生成物,分母为反应物,所以该方程式为:C(s)+H2O(g) ![]() CO(g)+H2(g) ,根据盖斯定律,①和②相加得此反应,△H= (a+b) kJ/mol ,因此,该反应的热化学方程式为: C(s)+H2O(g)
CO(g)+H2(g) ,根据盖斯定律,①和②相加得此反应,△H= (a+b) kJ/mol ,因此,该反应的热化学方程式为: C(s)+H2O(g) ![]() CO(g)+H2(g) △H= (a+b) kJ/mol ,根据化学方程式可知:K1=c2(CO)/c(CO2), K2=c(H2)
CO(g)+H2(g) △H= (a+b) kJ/mol ,根据化学方程式可知:K1=c2(CO)/c(CO2), K2=c(H2)![]() c(CO2)/c(CO)
c(CO2)/c(CO)![]() c(H2O) ,K3=
c(H2O) ,K3=![]() ,所以:K3= K1·K2 。
,所以:K3= K1·K2 。
(2)①根据图中平衡时H2O(g)的物质的量分数随温度的降低而增大,可知该反应正反应为放热反应,K随温度升高而减小,K随温度降低而增大。
②根据在密闭恒温(高于100℃)恒容装置中进行该反应CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g);可知A.混合气体密度不会改变,所以不能作为平衡的依据,故A错;B.由反应可知两边计量数不相等,混合气体压强不再改变标志达到平衡,故B正确;C.混合气体平均摩尔质量不再改变,M=m/n,说明n不再改变,说明达到平衡了,故C正确;D. n(CO2):n(H2)=1:2不符合化学平衡的定义,不能作为判断平衡的依据,故D错。本题答案:BC。
CH4(g)+2H2O(g);可知A.混合气体密度不会改变,所以不能作为平衡的依据,故A错;B.由反应可知两边计量数不相等,混合气体压强不再改变标志达到平衡,故B正确;C.混合气体平均摩尔质量不再改变,M=m/n,说明n不再改变,说明达到平衡了,故C正确;D. n(CO2):n(H2)=1:2不符合化学平衡的定义,不能作为判断平衡的依据,故D错。本题答案:BC。
③在密闭容器里全部由气体产于的反应中,平衡时气体压强之比=气体物质的量之比=气体物质的量浓度之比。根据200℃反应达到平衡时H2O(g)的物质的量分数,可知平衡时H2O(g)所占的压强为0.6p,根据化学方式可知CH4所占的压强为0.3p,因此CO2和H2所占的压强为0.1p。根据初始投料比以及CO2和H2化学计量数之比可知达到平衡时,两者的物质的量之比也为1:4,故平衡时CO2所占的压强为0.02p和H2所占的压强为0.08p,故可写出Kp的计算表达式为![]() 。
。
(3)①由图示已知吸收池用的是K2CO3溶液,吸收CO2,离子方程式为:CO32-+CO2+H2O=HCO3-,根据电荷守恒知 c(K+) + c(H+) == 2c(CO32-) + c(HCO3-) + c(OH-) ②已知惰性电极电解池中的电解液是KHCO3,阴极水放电生成氢气,阴极附近c(OH-)增大,OH-+HCO3-=CO32-+H2O,K+向阴极移动,使K2CO3溶液的得以再生。

【题目】硫酸锌被广泛应用于医药领域和工农业生产。工业上由氧化锌矿(主要成分为ZnO,另含ZnSiO3、FeCO3、CuO等)生产ZnSO47H2O的一种流程如图:
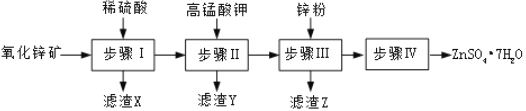
(1)步骤Ⅰ的操作是____________。
(2)步骤Ⅰ加入稀硫酸进行酸浸时,需不断通入高温水蒸气的目的是______________。
(3)步骤Ⅱ中,在pH约为5.1的滤液中加入高锰酸钾,生成Fe(OH)3和MnO(OH)2两种沉淀,该反应的离子方程式为____________________________________________。
(4)步骤Ⅲ中,加入锌粉的作用是______________。
(5)已知硫酸锌的溶解度与温度之间的关系如下表:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
从硫酸锌溶液中获得硫酸锌晶体的实验操作为________________、冷却结晶、过滤。烘干操作需在减压低温条件下进行,原因是_________________________________。
(6)取28.70 g ZnSO47H2O加热至不同温度,剩余固体的质量变化如图所示。分析数据,680℃时所得固体的化学式为______。
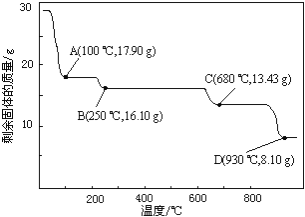
a.ZnO b.Zn3O(SO4)2 c.ZnSO4 d.ZnSO4H2O