题目内容
19.密闭的烧瓶里盛放气体A,在25℃时建立平衡:2A(g)?B(g)△H<0,把烧瓶置于100℃的沸水中,在建立新平衡的过程中,烧瓶内混合气体的物理量始终不变的是( )| A. | 平均相对分子质量 | B. | 密度 | ||
| C. | 容器内的压强 | D. | 物质的量 |
分析 升高温度,化学平衡向着吸热方向进行,而反应2A(g)?B(g)△H<0,向逆反应移动,混合物的物质的量增加,平均分子量减小,但是气体的总质量是守恒的,所以质量不变,所以总的物质的量增大,所以压强变小,气体的总质量是守恒的,烧瓶的体积也是不变的,所以密度不变,由此分析解答.
解答 解:A、升高温度,化学平衡向着吸热方向进行,而反应2A(g)?B(g)△H<0,向逆反应移动,物质的量变大,气体质量不变,所以相对分子量减少,故A错误;
B、气体的总质量是守恒的,烧瓶的体积也是不变的,所以密度不变,故B正确;
C、气体物质的量增强,所以压强变大,故C错误;
D、平衡逆向移动,所以物质的量增加,故D错误;
故选B.
点评 本题考查了温度对化学平衡的影响,题目难度中等,可以根据平衡移动原理判断温度对化学平衡的影响,试题侧重对学生灵活运用基础知识解决实际问题的能力的培养.

练习册系列答案
相关题目
9.比较锌和二氧化锰分别与盐酸的反应,下列叙述错误的是( )
| A. | 若Zn和MnO2都是足量的,则前一反应中盐酸全部被还原,后一反应中盐酸部分被氧化 | |
| B. | 两个都是氧化还原反应 | |
| C. | 盐酸都是被还原 | |
| D. | 等物质的量的Zn和MnO2分别与足量的浓盐酸反应,转移的电子数相等 |
10.下列物质的水溶液中不存在溶质分子的是( )
| A. | H2S | B. | HF | C. | HNO3 | D. | NH3•H2O |
7.莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法不正确的是( )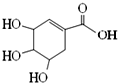

| A. | 分子式为C7H10O5 | |
| B. | 分子中含有3种官能团 | |
| C. | 可发生加成和取代反应 | |
| D. | 在水溶液中羟基和羧基均能电离出氢离子 |
14.下列说法中不正确的是( )
①将BaSO4放入水中不能导电,所以BaSO4是非电解质;
②氨溶于水得到的溶液能导电,所以氨水是电解质;
③固态的共价化合物不导电,熔融态的共价化合物可以导电;
④熔融的NaCl在电流作用下电离成Na+和Cl-;
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强;
⑥强电解质都是离子化合物,弱电解质都是共价化合物,
⑦强电解质的水溶液中不存在溶质分子.
①将BaSO4放入水中不能导电,所以BaSO4是非电解质;
②氨溶于水得到的溶液能导电,所以氨水是电解质;
③固态的共价化合物不导电,熔融态的共价化合物可以导电;
④熔融的NaCl在电流作用下电离成Na+和Cl-;
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强;
⑥强电解质都是离子化合物,弱电解质都是共价化合物,
⑦强电解质的水溶液中不存在溶质分子.
| A. | ①②③⑥ | B. | ①③⑤⑥⑦ | C. | ①②③④⑤⑥ | D. | 全部 |
4.下列说法正确的是( )
| A. | NH3的摩尔质量为17g | |
| B. | 48gO3含有的臭氧分子数为6.02×1023 | |
| C. | 1mol•L-1NaCl溶液中含1molNa+ | |
| D. | 标准状况下,1molH2O的体积为22.4 L |
 名称为3-甲基-2-丙基-1-戊烯.
名称为3-甲基-2-丙基-1-戊烯. 名称为1-甲基-3-乙基苯.
名称为1-甲基-3-乙基苯. 名称为:2,4-二甲基-3-乙基戊烷.
名称为:2,4-二甲基-3-乙基戊烷.