题目内容
3.戊醇C5H11OH与下列物质发生反应时,所得产物可能结构种数最少(不考虑立体异构)的是( )| A. | 与浓氢溴酸卤代 | B. | 与浓硫酸共热消去 | ||
| C. | 铜催化氧化 | D. | 与戊酸催化酯化 |
分析 A.醇发生溴代反应,官能团羟基被溴原子取代;
B.醇发生消去反应的条件是和羟基相连的邻碳含H原子;
C.醇催化氧化,羟基变成醛基或羰基,和羟基相连碳上无H得不能被氧化;
D.酯化反应羟基去氢,酸去羟基,剩余结合成酯.
解答 解:分子式为C5H11OH醇的同分异构体有:CH3CH2CH2CH2CH2OH;CH3CH2CH2CHOHCH3;CH3CH2CHOHCH2CH3;CH3CH(CH3)CH2CH2OH;CH3CH(CH3)CHOHCH3;CH3COH(CH3)CH2CH3;CH2OHCH(CH3)CH2CH3;CH3C(CH3)2CH2OH,共有8种情况.
A.醇发生溴代反应,官能团羟基被溴原子取代,所得产物种类和原醇相同;
B.醇发生消去反应的条件是和羟基相连的邻碳含H原子,通过消去反应得到的产物有CH2═CH-CH2-CH2-CH3、CH3-CH═CH-CH2-CH3、CH2═C(CH3)CH2CH3;CH3C(CH3)═CHCH3;CH3CH(CH3)CH═CH2共5种;
C.醇催化氧化,羟基变成醛基或羰基,和羟基相连碳上无H得不能被氧化,戊醇同分异构体中,只有CH3COH(CH3)CH2CH3不能被氧化,所得产物有7种;
D.酯化反应羟基去氢,酸去羟基,剩余结合成酯,所得产物和原醇类相同.
故所得产物异构体数目最少的为B,故选B.
点评 本题考查了同分异构体的判断,中等难度,搞清反应机理,才能正确判断产物种类.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
13.下列分子中的所有碳原子不可能处在同一平面上的是( )
① ②
② ③
③ ④
④ ⑤CH3CH=CHCH3.
⑤CH3CH=CHCH3.
①
 ②
② ③
③ ④
④ ⑤CH3CH=CHCH3.
⑤CH3CH=CHCH3.| A. | ②③ | B. | ①④ | C. | ①②④ | D. | ①⑤ |
14.下列图示实验正确的是( )
| A. |  | B. |  | C. |  | D. |  |
11.如图图象与对应的叙述相符的是( )

| A. | 图I表示盐酸滴加到0.1mol/L某碱溶液中得到的滴定曲线,由图I可知二者恰好中和时,所得溶液的pH=7 | |
| B. | 图II表示一定条件下进行的反应2SO2+O2?2SO3△H<0各成分的物质的量变化,t2时刻改变的条件可能是加压或降低温度 | |
| C. | 图III表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20ml Ba(OH)2溶液时,沉淀是Al(OH)3与BaSO4的混合物 | |
| D. | 图IV表示向一定体积含等浓度NH4Cl、AlCl3、MgCl2混合溶液中逐渐加入NaOH溶液至过量的过程中,生成沉淀的质量与加入NaOH溶液的体积之间的关系 |
18.下列有关物质的实验操作、现象及结论描述正确的是( )
| 选项 | 实验操作及现象 | 结论 |
| A | 用铂丝蘸取某待测液在酒精灯外焰上灼烧,火焰呈紫色(透过蓝色钴玻璃) | 待测试液中一定含有钾元素,可能含钠元素 |
| B | 向某无色溶液中通入过量的CO2气体,有白色沉淀产生 | 该溶液中一定含有SiO32- |
| C | 向品红溶液中通入某气体后,溶液褪色 | 该气体一定是SO2 |
| D | 向NaOH溶液中滴加MgCl2溶液,产生白色沉淀,继续滴加FeCl3溶液产生红褐色沉淀 | Fe(OH)3的溶解度大于Mg(OH)2的溶解度 |
| A. | A | B. | B | C. | C | D. | D |
8.将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一.一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺流程提取其他产品.
回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是②③④(填序号).
①用混凝法获取淡水
②提高部分产品的质量
③优化提取产品的品种
④改进钾、溴、镁等的提取工艺
(2)采用“空气吹出法”从浓海水吹出Br2,并用纯碱吸收.已知该反应不产生CO2,且溴歧化为Br-和BrO3-,则反应的离子反应方程式为3Br2+6CO32-+3H2O=5Br-+BrO3-+6HCO3-.
(3)海水提镁的一段工艺流程如图:
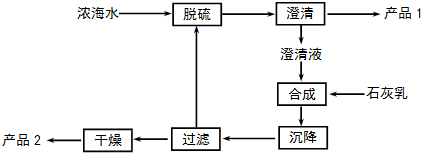
浓海水的主要成分如下:
该工艺过程中,脱硫阶段主要反应的阳离子Ca2+,沉降阶段反应的离子方程式为Mg2+(aq)+Ca(OH)2(s)=Mg(OH)2(s)+Ca2+(aq),浓海水的利用率为90%,则1L浓海水最多可得到产品2的质量为62.64g.
(4)由MgCl2•6H2O制备MgCl2固体时是在氯化氢气体氛围中加热进行,其目的是抑制MgCl2水解.
回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是②③④(填序号).
①用混凝法获取淡水
②提高部分产品的质量
③优化提取产品的品种
④改进钾、溴、镁等的提取工艺
(2)采用“空气吹出法”从浓海水吹出Br2,并用纯碱吸收.已知该反应不产生CO2,且溴歧化为Br-和BrO3-,则反应的离子反应方程式为3Br2+6CO32-+3H2O=5Br-+BrO3-+6HCO3-.
(3)海水提镁的一段工艺流程如图:

浓海水的主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
(4)由MgCl2•6H2O制备MgCl2固体时是在氯化氢气体氛围中加热进行,其目的是抑制MgCl2水解.
15.某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol•L-1的盐酸,测得溶液中的HCO3-、CO32-、AlO2-、Al3+离子的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是( )

| A. | 原混合溶液中的CO32-与AlO2-的物质的量之比为1:2 | |
| B. | V1:V2=l:5 | |
| C. | M点时生成的CO2为0.05mol | |
| D. | e曲线表示的离子方程式为:Al(OH)3+3H+=Al3++3H2O |
12.下列判断正确的是( )
| A. | HClO4、H2SO4、CH3COOH、H2CO3酸性依次减弱 | |
| B. | Cl-、Na+、Mg2+、F-的半径依次减小 | |
| C. | Na、Mg、Al失电子能力随最外层电子的增加而增强 | |
| D. | HI、HBr、HCl、HF的沸点依次降低 |
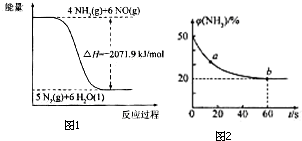 合理应用和处理氮的化合物,在生产生活中有重要意义.
合理应用和处理氮的化合物,在生产生活中有重要意义.