题目内容
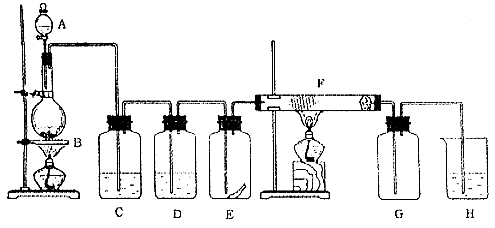
下图为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质实验的装置。其中E瓶中放
有干燥红色布条;F中为铜网,右端为一团棉花。
|
|
 试回答:
试回答:(1)仪器A的名称叫 ,烧瓶B中反应的化学方程式为_____________ ,
(2)C中试剂是 ;D中试剂的作用是 ;
(3)E中现象是 ; F中反应的化学方程式是 ,
(4)H中发生反应的化学方程式为 。
(1)分液漏斗 MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O (2)饱和食盐水;干燥氯气;
MnCl2+Cl2↑+2H2O (2)饱和食盐水;干燥氯气;
(3)布条不褪色;Cu+Cl2 CuCl2 (4)Cl2+2NaOH=NaCl+NaClO+H2O
CuCl2 (4)Cl2+2NaOH=NaCl+NaClO+H2O
(10分。方程式每空2分,其余每空1分)
解析试题分析:根据题中所给出的信息可知本实验是室制取纯净、干燥的Cl2,并进行检验Cl2性质实验。
(1)根据仪器的结构特点可知,仪器A是分液漏斗。依据课本所学制备氯气用的是浓盐酸和固体MnO2的加热反应.所以A中为浓盐酸,B中为MnO2,因此烧瓶B中反应的化学方程式为MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(2)由于浓盐酸易挥发,所以生成氯气中含有挥发出的HCl气体,除去HCl气体用饱和食盐水,因此C中试剂为饱和食盐水;要验证氯气的干燥性,需要干燥氯气。而氯气含有水蒸气,所以D中盛放的是浓硫酸,用来干燥氯气。
(3)氯气从D中出来后是干燥的氯气,通到E中,干燥的氯气没有漂白性,因此E中的干燥布条不褪色;已知F中是铜网,在加热的条件下,氯气与Cu发生反应,生成棕黄色的烟,反应的化学方程式为Cu+Cl2 CuCl2。
CuCl2。
(4)氯气是有毒气体,属于大气污染物,需要尾气处理。所以H中是吸收多余氯气的NaOH溶液,反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O。
考点:考查氯气制备、除杂、氯气性质检验、仪器识别以及尾气处理等

 初中学业考试导与练系列答案
初中学业考试导与练系列答案某学校兴趣小组设计如下装置进行实验探究(a、b为弹簧夹,加热及固定装置已略去)。
(1)验证碳、硅非金属性的相对强弱
①连接仪器、 、加药品后,打开a关闭b,然后滴入浓硫酸,加热;
②装置A中的试剂是 ;
③能说明碳的非金属性比硅强的实验现象是 。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性
①打开b,关闭a。能验证SO2具有氧化性的化学方程式是 ;
②若过量的SO2通入NaOH溶液中,其离子方程式是 ;
③BaCl2溶液中无沉淀现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | | |
写出其中SO2显示还原性并生成沉淀的离子方程式 。
根据下列框图,有关说法正确的是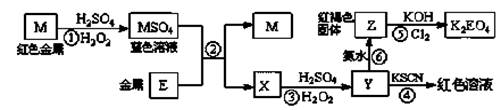
| A.M、E都是第四周期中的过渡元素,E的金属活动性比M的金属活动性强,E3+的氧化性比M2+的氧化性弱 |
| B.反应⑤的离子方程式可表示为:2E(OH)3 +3Cl2 +6H2O =3EO4 2―+ 6Cl― +12H+ |
| C.反应①、②、③、⑤都属于氧化还原反应,且在反应①和③中硫酸仅表现了酸性 |
| D.用K2EO4、Zn可制成一种高能电池,该电池中负极的电极反应式为: |
 KClO3+5KCl+3H2O )
KClO3+5KCl+3H2O )




 Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O