题目内容
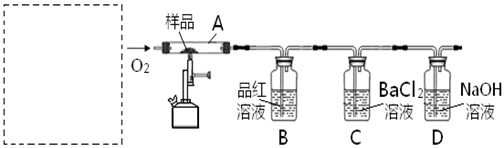
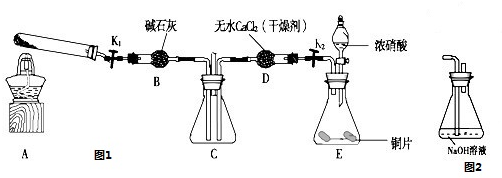
亚硝酸钠(NaNO2)暴露于空气中会与氧气反应生成硝酸钠,在纤维纺织品的染色和漂白、照相、生产橡胶、制药等领域有广泛应用,也常用于鱼类、肉类等食品的染色和防腐。但因其有毒,所以在食品行业用量有严格限制。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物成分。
已知:①NO+NO2+2OH—==2NO2—+H2O ②气体液化的温度:NO2:21℃,NO:-152℃
(1)为了检验装置A中生成的气体产物,仪器的连接顺序(按左→右连接):A、C、 、 、 。
(2)反应前应打开弹簧夹,先通人一段时间氮气,排除装置中的空气,目的是 。
(3)在关闭弹簧夹,打开分液漏斗活塞,滴人70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是 。
②装置E的作用是 。
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为 。如果没有装置C,对实验结论造成的影响是 。
(5)通过上述实骏探究过程,可得出装置A中反应的化学方程式是 。
(1)E、D、B(2)防止可能生成的NO被氧化成NO2,造成对A中反应气体产物检验造成干扰
(3)①D中通入氧气后,出现红棕色气体 ②冷凝,使NO2完全液化
(44NO+O2+4NaOH=2H2O+4NaNO3水蒸气存在,会与NO2反应产生NO,造成对NO的来源认识不清
(5)2NaNO2+H2SO4 NO↑+NO2↑+Na2SO4+H2O。
NO↑+NO2↑+Na2SO4+H2O。
解析试题分析:(1)在A装置中可能发生的反应有:2NaNO2+H2SO4(浓)  Na2SO4+2HNO2,2HNO2
Na2SO4+2HNO2,2HNO2 NO↑+NO2↑+H2O。由于气体液化的温度:NO2:21℃,NO:-152℃,所以NO2首先液化,要先用E检验,然后用D装置根据2NO+O2= 2NO2无色气体变为红棕色来验证NO的存在。NO、NO2都是大气污染物,最后要进行尾气处理,用B装置的NaOH溶液来吸收。为了检验装置A中生成的气体产物,仪器的连接顺序是 A、C、E、D、B。(2)反应前应打开弹簧夹,先通人一段时间氮气,排除装置中的空气,是为了防止可能生成的NO被氧化成NO2,造成对A中反应气体产物检验造成干扰。
NO↑+NO2↑+H2O。由于气体液化的温度:NO2:21℃,NO:-152℃,所以NO2首先液化,要先用E检验,然后用D装置根据2NO+O2= 2NO2无色气体变为红棕色来验证NO的存在。NO、NO2都是大气污染物,最后要进行尾气处理,用B装置的NaOH溶液来吸收。为了检验装置A中生成的气体产物,仪器的连接顺序是 A、C、E、D、B。(2)反应前应打开弹簧夹,先通人一段时间氮气,排除装置中的空气,是为了防止可能生成的NO被氧化成NO2,造成对A中反应气体产物检验造成干扰。
(3)①D中气体是无色的,当通入氧气后,出现红棕色气体。②装置E的作用是冷凝,使NO2完全液化
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为4NO+O2+4NaOH=2H2O+4NaNO3如果没有装置C,产生的气体中含有的水蒸气,就会与NO2发生反应:3NO2+H2O=2HNO3+NO。产生了NO,造成对NO的来源认识不清。影响判断结果的正确性。(5)通过上述实骏探究过程,可得出装置A中反应的化学方程式是2NaNO2+H2SO4(浓)  Na2SO4+2HNO2,2HNO2
Na2SO4+2HNO2,2HNO2 NO↑+ NO2↑ +H2O。叠加得到总方程式为:2NaNO2+H2SO4
NO↑+ NO2↑ +H2O。叠加得到总方程式为:2NaNO2+H2SO4 NO↑+NO2+Na2SO4+H2O
NO↑+NO2+Na2SO4+H2O
考点:考查

为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。
实验Ⅰ 反应产物的定性探究
实验装置如图所示。(固定装置已略去)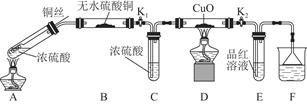
(1)A中反应的化学方程式为 。
(2)F烧杯中的溶液通常是 。
(3)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是 。
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是 。
(5)为说明浓硫酸中的水是否影响B装置现象的判断,还须进行一次实验。实验方案为 。
实验Ⅱ 反应产物的定量探究
(6)在铜与浓硫酸反应的过程中,发现有黑色物质出现,经查阅文献获得下列资料。
资料1:
| 硫酸/mol·L-1 | 黑色物质出现的温度/℃ | 黑色物质消失的温度/℃ |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
资料2:X射线晶体分析表明,铜与浓硫酸反应生成的黑色物质为Cu2S、CuS、Cu7S4中的一种或几种。仅由上述资料可得出的正确结论是 __。
a.铜与浓硫酸反应时所涉及的反应可能不止一个
b.硫酸浓度选择适当,可避免最后产物中出现黑色物质
c.该反应发生的条件之一是硫酸浓度≥15 mol·L-1
d.硫酸浓度越大,黑色物质越快出现、越难消失
(7)为测出硫酸铜的产率,将该反应所得溶液中和后配制成250.00 mL溶液,取该溶液25.00 mL加入足量KI溶液振荡,以淀粉溶液为指示剂,用b mol·L-1Na2S2O3溶液滴定生成的I2,3次实验平均消耗该Na2S2O3溶液V mL。若反应消耗铜的质量为a g,则硫酸铜的产率为 _。(已知:2Cu2++4I-=2CuI+I2,2S2O32-+I2=S4O62-+2I-)
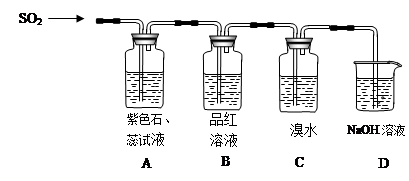
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题。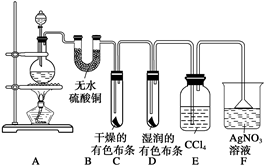
(1)下列方法中,可制得氯气的正确组合是 。
①MnO2和浓盐酸混合共热
②KMnO4和浓盐酸混合 ③氯酸钠和浓盐酸混合 ④K2Cr2O7和浓盐酸混合
| A.①②③ | B.①②④ | C.①② | D.全部可以 |
(3)①装置B的作用是 ,现象是 。
②装置C和D出现的不同现象说明的问题是 。
③装置E的作用是
目前我国饮用水消毒主要用氯——通氯气,加漂白粉或漂白精。
(1) 漂白粉或漂白精长期放置于空气中会变质失效,其化学方程式是__________________。
(2)目前我国广泛采用经过干燥空气稀释的氯气,通入填有固体亚氯酸钠(NaClO2)的柱内
制得ClO2,这一反应的化学方程式是:_________________________________________。
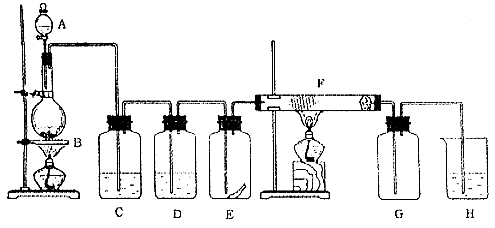
下图为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质实验的装置。其中E瓶中放
有干燥红色布条;F中为铜网,右端为一团棉花。
|
|
 试回答:
试回答:(1)仪器A的名称叫 ,烧瓶B中反应的化学方程式为_____________ ,
(2)C中试剂是 ;D中试剂的作用是 ;
(3)E中现象是 ; F中反应的化学方程式是 ,
(4)H中发生反应的化学方程式为 。
 2KNO2↑+O2↑
2KNO2↑+O2↑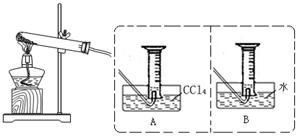

 CaO+CO2 ㈡ 2CaO+2SO2+O2 =2CaSO4
CaO+CO2 ㈡ 2CaO+2SO2+O2 =2CaSO4