题目内容
6.有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大.A原子核内无中子;A和E、D和F分别同主族,且B与D 最外层电子数之比为2:3.试回答下列问题:
(1)A元素的名称是氢,E元素在周期表中的位置是第三周期ⅠA族;
(2)C、D、F的气态氢化物稳定性由强到弱的顺序是H2O>NH3>H2S(填化学式);
(3)E单质在足量D单质中燃烧生成的化合物的电子式是
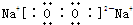 ;
;(4)化合物X、Y均由A、D、E、F四种元素组成.
①X、Y中存在的化学键类型是离子键、共价键;
②X与Y的水溶液相混合发生反应的离子方程式为H++HSO3-=H2O+SO2↑;
(5)向化合物E2F的水溶液中滴入双氧水和稀硫酸,加热,有单质生成.其离子反应方程式为:S2-+H2O2+2H+═S↓+2H2O;
(6)若由A、C组成的简单氢化物燃烧生成无污染物,燃烧热为aKJ/mol,请写出表示该简单氢化物燃烧热的热化学方程式NH3(g)+$\frac{3}{4}$O2(g)═$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2O(l);△H=-aKJ/mol.
分析 A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A原子核内无中子,则A为H元素;A和E同主族,结合原子序数可知E为Na;B与D最外层电子数之比为2:3,由原子序数可知,二者都处于第二周期且不相邻,故B、D原子最外层电子数分别为4、6,可推知B为C元素、D为O元素,则C为N元素;D和F同主族,则F为S元素,据此进行解答.
解答 解:A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大.A原子核内无中子,则A为H元素;A和E同主族,结合原子序数可知E为Na;B与D最外层电子数之比为2:3,由原子序数可知,二者都处于第二周期且不相邻,故B、D原子最外层电子数分别为4、6,可推知B为C元素、D为O元素,则C为N元素;D和F同主族,则F为S元素,
(1)由上述分析可知,A为氢元素;E为Na元素,处于周期表中第三周期ⅠA族,
故答案为:氢;第三周期ⅠA族;
(2)非金属性O>N>S,故N、O、S元素氢化物的稳定性H2O>NH3>H2S,
故答案为:H2O>NH3>H2S;
(3)Na单质在足量氧气中燃烧生成的化合物为Na2O2,其电子式为: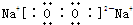 ,
,
故答案为: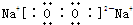 ;
;
(4)化合物X、Y均由H、O、Na、S四种元素组成,分别为NaHSO3、NaHSO4中的一种,
①NaHSO3、NaHSO4均属于离子化合物,二者中都含有离子键和共价键;
②X与Y的水溶液相混合发生反应的离子方程式为:H++HSO3-=H2O+SO2↑;
故答案为:离子键、共价键;H++HSO3-=H2O+SO2↑;
(5)化合物Na2S的水溶液中滴入双氧水和稀硫酸,加热,生成单质为S,同时生成水,其反应离子方程式为:S2-+H2O2+2H+=S↓+2H2O,
故答案为:S2-+H2O2+2H+=S↓+2H2O;
(6)若由A、C组成的简单氢化物为氨气,氨气燃烧生成无污染物,该产物应该为氮气,氨气的燃烧热为aKJ/mol,则氨气燃烧热的热化学方程式为:NH3(g)+$\frac{3}{4}$O2(g)═$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2O(l);△H=-aKJ/mol,
故答案为:NH3(g)+$\frac{3}{4}$O2(g)═$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2O(l);△H=-aKJ/mol.
点评 本题考查结构性质位置关系综合应用、常用化学用语等知识,题目难度中等,推断元素是解题关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系.

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案| A. | H2SO4 | B. | NaNO3 | C. | KOH | D. | MgO |
| A. | 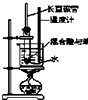 实验室制硝基苯 | B. |  石油分馏 | ||
| C. |  实验室用酒精制取乙烯 | D. | 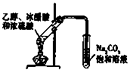 实验室制乙酸乙酯 |
| A. | 制备硝基苯,混合药品的顺序为:向试管中先加入苯,再加入浓硫酸,最后加入浓硝酸 | |
| B. | 银镜反应、乙醛与新制Cu(OH)2反应、实验室制取乙烯都必须用水浴加热 | |
| C. | 在重结晶的实验中,使用长颈漏斗趁热过滤是为了减少被提纯物质的损失 | |
| D. | 苯甲酸的重结晶实验中要得到纯净的苯甲酸固体需要进行至少两次过滤操作 |
| A. | 3种 | B. | 5种 | C. | 6种 | D. | 7 种 |
| A. | 用铜和稀硫酸反应制取硫酸铜溶液 | |
| B. | 用石灰石除去氯化钙溶液中混有的盐酸 | |
| C. | 用氢氧化钠溶液除去二氧化碳中混有的氯化氢气体 | |
| D. | 用酚酞试液检验暴露在空气中的NaOH固体是否变质 |
| A. | 三氯化硼液态时能导电而固态时不导电 | |
| B. | 三氯化硼加到水中使溶液的pH升高 | |
| C. | 三氯化硼分子呈正三角形,属非极性分子 | |
| D. | 分子中所有原子都满足最外层8电子稳定结构 |