题目内容
 某无色稀溶液X中,可能含有下表所列离子中的某几种.
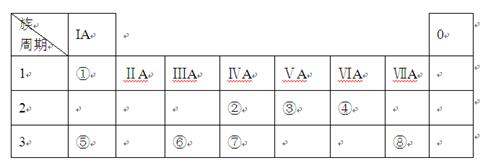
某无色稀溶液X中,可能含有下表所列离子中的某几种.| 阴离子 | CO32-、SiO32-、AlO2-、Cl- |
| 阳离子 | Al3+、Cu2+、Mg2+、NH4+、Na+ |
(1)若Y是盐酸,则溶液中含有的金属阳离子是
Na+
Na+
,ab段发生反应的总离子方程式为CO32-+2H+=H2O+CO2↑
CO32-+2H+=H2O+CO2↑
,Oa段上表中参加反应的离子的物质的量之比为n(SiO32- ):n(AlO2-)=11:2
n(SiO32- ):n(AlO2-)=11:2
[要标明离子符号,如n(Na+)].(2)若Y是NaOH溶液,则bc段反应的离子方程式为
Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
.若不考虑离子的水解因素,忽略H+和OH-影响,且溶液中只存在四种离子,则它们的离子个数比为N(Al3+):N(Mg2+ ):N(NH4+)、N(Cl- )=2:1:4:12
N(Al3+):N(Mg2+ ):N(NH4+)、N(Cl- )=2:1:4:12
[按阳离子在前,阴离子在后,高价在前,低价在后的顺序排列].分析:溶液无色说明溶液中不含铜离子;
(1)如果Y是盐酸,向溶液中加盐酸,先生成沉淀,当a-b段时,沉淀的量不变化,盐酸和碳酸根离子反应生成气体,则溶液中不含镁离子、铝离子;当b-c段时沉淀的质量减少,部分沉淀和盐酸反应,部分沉淀和盐酸不反应,说明溶液中有硅酸根离子和偏铝酸根离子,弱酸根离子和铵根离子能双水解,所以溶液中含有的阳离子是钠离子;
(2)若Y是氢氧化钠,向溶液中加氢氧化钠溶液,先生成沉淀,当a-b段时,沉淀的量不变化,氢氧化钠和铵根离子反应生成气体;当b-c段时沉淀的质量减少,部分沉淀和氢氧化钠反应,部分沉淀不反应,说明溶液中有铝根离子和镁离子,则溶液中不含硅酸根离子、碳酸根离子和偏铝酸根离子,所以溶液中含有的阴离子是氯离子.
(1)如果Y是盐酸,向溶液中加盐酸,先生成沉淀,当a-b段时,沉淀的量不变化,盐酸和碳酸根离子反应生成气体,则溶液中不含镁离子、铝离子;当b-c段时沉淀的质量减少,部分沉淀和盐酸反应,部分沉淀和盐酸不反应,说明溶液中有硅酸根离子和偏铝酸根离子,弱酸根离子和铵根离子能双水解,所以溶液中含有的阳离子是钠离子;
(2)若Y是氢氧化钠,向溶液中加氢氧化钠溶液,先生成沉淀,当a-b段时,沉淀的量不变化,氢氧化钠和铵根离子反应生成气体;当b-c段时沉淀的质量减少,部分沉淀和氢氧化钠反应,部分沉淀不反应,说明溶液中有铝根离子和镁离子,则溶液中不含硅酸根离子、碳酸根离子和偏铝酸根离子,所以溶液中含有的阴离子是氯离子.
解答:解:溶液无色说明溶液中不含铜离子;
(1)如果Y是盐酸,向溶液中加盐酸,先生成沉淀,当a-b段时,沉淀的量不变化,盐酸和碳酸根离子反应生成气体,则溶液中不含镁离子、铝离子;当b-c段时沉淀的质量减少,部分沉淀和盐酸反应,部分沉淀和盐酸不反应,说明溶液中有硅酸根离子和偏铝酸根离子,弱酸根离子和铵根离子能双水解,所以溶液中含有的阳离子是钠离子.
通过以上分析知,溶液中含有的阳离子是钠离子,ab段发生反应是碳酸根离子和氢离子反应生成二氧化碳和水,离子方程式为:CO32-+2H+=H2O+CO2↑;根据图象知,氢氧化铝和盐酸反应需要1v盐酸,偏铝酸根离子和硅酸根离子和盐酸反应需要盐酸4V盐酸,有关反应方程式为:AlO2-+H++H2O=Al(OH)3↓、SiO32-+2H+=H2SiO3 ↓、Al(OH)3+3H+=Al3++3H2O,根据方程式知,SiO32-生成H2SiO3需要盐酸的体积与AlO2-生成Al(OH)3 需要盐酸的体积之比=
:
=11:2,
故答案为:Na+;CO32-+2H+=H2O+CO2↑;11:2;
(2)若Y是氢氧化钠,向溶液中加氢氧化钠溶液,先生成沉淀,当a-b段时,沉淀的量不变化,氢氧化钠和铵根离子反应生成气体;当b-c段时沉淀的质量减少,部分沉淀和氢氧化钠反应,部分沉淀不反应,说明溶液中有铝根离子和镁离子,则溶液中不含硅酸根离子、碳酸根离子和偏铝酸根离子,所以溶液中含有的阴离子是氯离子.
Y是NaOH溶液,则bc段是氢氧化铝和氢氧化钠反应生成偏铝酸钠和水,离子方程式为:Al(OH)3+OH-=AlO2-+2H2O;
和铵根离子需要氢氧化钠的体积是2v,氢氧化铝和氢氧化钠反应需要氢氧化钠的体积是1v,则生成氢氧化铝需要氢氧化钠的体积是3V,生成氢氧化镁需要氢氧化钠的体积是1V,则n(Al3+):n(Mg2+):n(NH4+)=1:
:2=2:1:4,溶液中阴阳离子所带电荷相等知,n(Al3+):n(Mg2+ ):n(NH4+)、n(Cl- )=2:1:4:12,即N(Al3+):N(Mg2+ ):N(NH4+)、N(Cl- )=2:1:4:12,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;N(Al3+):N(Mg2+ ):N(NH4+)、N(Cl- )=2:1:4:12.
(1)如果Y是盐酸,向溶液中加盐酸,先生成沉淀,当a-b段时,沉淀的量不变化,盐酸和碳酸根离子反应生成气体,则溶液中不含镁离子、铝离子;当b-c段时沉淀的质量减少,部分沉淀和盐酸反应,部分沉淀和盐酸不反应,说明溶液中有硅酸根离子和偏铝酸根离子,弱酸根离子和铵根离子能双水解,所以溶液中含有的阳离子是钠离子.
通过以上分析知,溶液中含有的阳离子是钠离子,ab段发生反应是碳酸根离子和氢离子反应生成二氧化碳和水,离子方程式为:CO32-+2H+=H2O+CO2↑;根据图象知,氢氧化铝和盐酸反应需要1v盐酸,偏铝酸根离子和硅酸根离子和盐酸反应需要盐酸4V盐酸,有关反应方程式为:AlO2-+H++H2O=Al(OH)3↓、SiO32-+2H+=H2SiO3 ↓、Al(OH)3+3H+=Al3++3H2O,根据方程式知,SiO32-生成H2SiO3需要盐酸的体积与AlO2-生成Al(OH)3 需要盐酸的体积之比=
4-
| ||
| 2 |
| 1 |
| 3 |
故答案为:Na+;CO32-+2H+=H2O+CO2↑;11:2;
(2)若Y是氢氧化钠,向溶液中加氢氧化钠溶液,先生成沉淀,当a-b段时,沉淀的量不变化,氢氧化钠和铵根离子反应生成气体;当b-c段时沉淀的质量减少,部分沉淀和氢氧化钠反应,部分沉淀不反应,说明溶液中有铝根离子和镁离子,则溶液中不含硅酸根离子、碳酸根离子和偏铝酸根离子,所以溶液中含有的阴离子是氯离子.
Y是NaOH溶液,则bc段是氢氧化铝和氢氧化钠反应生成偏铝酸钠和水,离子方程式为:Al(OH)3+OH-=AlO2-+2H2O;
和铵根离子需要氢氧化钠的体积是2v,氢氧化铝和氢氧化钠反应需要氢氧化钠的体积是1v,则生成氢氧化铝需要氢氧化钠的体积是3V,生成氢氧化镁需要氢氧化钠的体积是1V,则n(Al3+):n(Mg2+):n(NH4+)=1:
| 1 |
| 2 |
故答案为:Al(OH)3+OH-=AlO2-+2H2O;N(Al3+):N(Mg2+ ):N(NH4+)、N(Cl- )=2:1:4:12.
点评:本题考查了溶液中离子的判断,能明确离子的性质是解本题的关键,会根据图象确定溶液中存在的离子及其含量,难度不大.

练习册系列答案
相关题目
(1)锡为第ⅣA族元素,锡的单质和化合物与某些物质的化学性质有许多相似之处。已知锡元素具有如下性质:
 ;
;




 。
。
试回答:
①锡溶于盐酸,再向反应后的溶液中通入氯气,有关反应类似于铁的相应变化,试写出有关反应的化学方程式:_____________________________________________________,_______________________________________。
②将①中溶液蒸干后继续灼烧所得固体,变化过程类似于FeCl3溶液相应的变化,则最后得到的固体物质是__________(填化学式)。
③若可用SnCl2溶液与过量的碱溶液反应的方法制Sn(OH)2,该碱可选用________。
(2)某无色稀溶液X中,可能含有下表所列离子中的某几种。
|
阴离子 |
|
|
阳离子 |
|
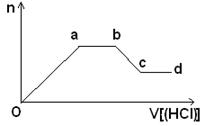
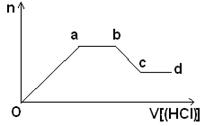
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂Y体积(V)的关系如图所示。

①若Y是盐酸,则溶液中含有的金属阳离子是_________,ab段发生反应的离子方程式为_______________,图中oa段参加反应的阴离子的物质的量之比为___________________。
②若Y是NaOH溶液,则bc段反应的离子方程式为____________________。
若不考虑离子的水解,忽略H+和OH-的影响,且溶液中只存在四种离子,则它们的离子个数比为_____________________________________________(按阳离子在前,阴离子在后,高价在前,低价在后的顺序排列)。
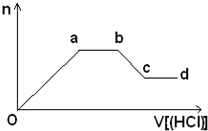 下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题: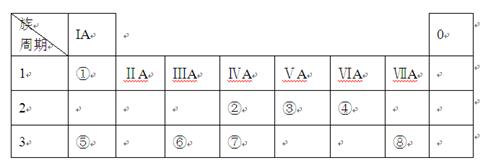
 (2)②、③、⑦元素的最高价含氧酸的酸性由强到弱的顺序是 。
(2)②、③、⑦元素的最高价含氧酸的酸性由强到弱的顺序是 。