题目内容
【题目】储氢作为氢能利用的关键技术,是当前关注的热点之一。一定条件下,如图所示装置可实现有机物的电化学储氢(忽略其他有机物).下列说法错误的是( )
已知:电流效率(η=![]() ×100%)
×100%)
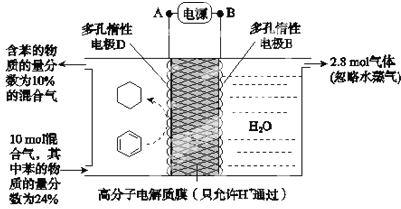
A.电源B为正极
B.导线中电子移动方向为A→D
C.电极D反应式为C6H6+6H++6e-=C6H12
D.该储氢装置的电流效率η=24.3%
【答案】D
【解析】
A. 根据分析苯在左侧变为环己烷,化合价减低,发生还原反应,即为阴极,因此电源A为负极,电源B为正极,故A正确;
B. 根据A选项分析得到电源A为负极,导线中电子移动方向从负极即A极→阴极即D极,故B正确;
C. 电极D是苯变为环己烷,其电极反应式为C6H6 + 6H+ + 6e- = C6H12,故D正确;
D. 阳极得到2.8mol氧气,则电子转移为2.8mol×4 = 11.2mol,阴极10mol混合气体中苯物质的量分数由24%变为10%,则反应了10×(24% 10%) = 1.4mol,则得到电子物质的量为1.4mol×6 = 8.4mol,因此该储氢装置的电流效率![]() ,故D错误。
,故D错误。
综上所述,答案为D。

练习册系列答案
相关题目
【题目】下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)
A | B | C | D |
NaCl溶于水 |
电解CuCl2溶液 |
CH3COOH在水中电离 |
H2与Cl2反应能量变化 |
NaCl | CuCl2 | CH3COOH | H2(g)+Cl2(g) ΔH=183kJ·mol1 |
A. AB. BC. CD. D