题目内容
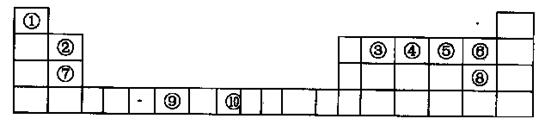
A-E是周期表中1一36号的元素,它们的原子序数依次递增且分别位于前四周期的各个周期中。对它们的性质及结构的描述如下。
A原子的基态只有一种形状的电子云,并容易形成共价键;B原子的最外电子层的电子排布可表示为nsnnpn,其元素最高正化合价与最低负化合价的代数和为0;C与B同周期,其第一电离能髙于周期表中与之相邻的所有元素;D元素在周期表中位于C元素的下一周期,其电负性在同周期元素中最大;E原子最外电子层只有未成对电子,其内层所有轨道全部充满,但并不是第IA族元素。
(1)请写出E原子基态的电子排布式____________。
(2)A与C形成的最简单化合物(甲)分子的立体结构是____________,其中C原子的杂化方式是______
(3)A与D元素形成的化合物(乙)与甲相比,沸点较低的是(写化学式)____________原因是________________________
(4)B元素可形成B70单质,它在一定条件下吸收可见光后可高效杀灭癌细胞,有望成为癌症治疗药物的候选材料。它与金属钾掺杂在一起的化合物,其晶胞如图所示(白球位于立方体的体心和顶点,小黑球位于立方体的面上),则该化合物中B70与钾原子个数比为______。

A原子的基态只有一种形状的电子云,并容易形成共价键;B原子的最外电子层的电子排布可表示为nsnnpn,其元素最高正化合价与最低负化合价的代数和为0;C与B同周期,其第一电离能髙于周期表中与之相邻的所有元素;D元素在周期表中位于C元素的下一周期,其电负性在同周期元素中最大;E原子最外电子层只有未成对电子,其内层所有轨道全部充满,但并不是第IA族元素。
(1)请写出E原子基态的电子排布式____________。
(2)A与C形成的最简单化合物(甲)分子的立体结构是____________,其中C原子的杂化方式是______
(3)A与D元素形成的化合物(乙)与甲相比,沸点较低的是(写化学式)____________原因是________________________
(4)B元素可形成B70单质,它在一定条件下吸收可见光后可高效杀灭癌细胞,有望成为癌症治疗药物的候选材料。它与金属钾掺杂在一起的化合物,其晶胞如图所示(白球位于立方体的体心和顶点,小黑球位于立方体的面上),则该化合物中B70与钾原子个数比为______。

(8分)
(1)1s22s22p63s23p63d104s1或[Ar]3d104s1(2分)
(2)三角锥形(1分);sp3杂化(1分)
(3)HCl(1分);NH3分子之间存在氢键,HCl分子间不存在氢键(1分)
(4)1:3(2分)
(1)1s22s22p63s23p63d104s1或[Ar]3d104s1(2分)
(2)三角锥形(1分);sp3杂化(1分)
(3)HCl(1分);NH3分子之间存在氢键,HCl分子间不存在氢键(1分)
(4)1:3(2分)
试题分析:A原子的基态只有一种形状的电子云,容易形成共价键为H;B原子的最外电子层的电子排布可表示为nsnnpn,其元素最高正化合价与最低负化合价的代数和为0,最外层4个电子,说明n=2,为C;C与B同周期,其第一电离能髙于周期表中与之相邻的所有元素,推断只能为N;第三周期电离能最大的D为Cl;在第四周期,最外层1个电子只有K、Cu,排除K,E是Cu。
(1)Cu电子排布式:1s22s22p63s23p63d104s1。
(2)NH3分子的立体结构是:三角锥形;中心原子N的价层电子对数(5+3)/2=4,为sp3杂化。
(3)由于NH3分子间存在氢键,熔沸点较高。
(4)结合晶胞图像可知B70共1/8×8+1=2个,钾原子个数1/2×2×6=6个。

练习册系列答案
相关题目

 的立体构型是 。
的立体构型是 。

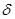 键与
键与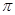 键的个数比为 。
键的个数比为 。
