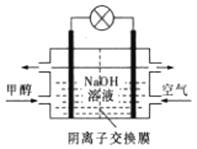
题目内容
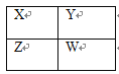
【题目】如图所示为元素周期表的一部分,下列说法中正确的是( )
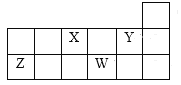
A.Z元素的最高价氧化物对应的水化物能与X的最简单气态氢化物的水溶液反应
B.X、Y、Z、W元素形成的简单离子半径由小到大的顺序为Z<X<Y<W
C.W的最简单气态氢化物的水溶液能与其最高价氧化物对应的水化物反应生成W元素对应的单质
D.X、Z两种元素的氧化物中所含化学键的类型相同
【答案】C
【解析】
从周期表结构分析,X是N,Y是F,Z是Al,W是S;
A.Al元素的最高价氧化物对应的水化物是Al(OH)3,N的最简单气态氢化物为NH3,其水溶液是氨水;
B.X、Y、Z、W元素形成的简单离子为:N3-、F-、Al3+、S2-;
C.S的最简单气态氢化物为H2S,高价氧化物对应的水化物为H2SO4;
D.N的氧化物有NO、NO2等,Al的氧化物是Al2O3;
据此解答。
A.氨水是弱碱,不能和Al(OH)3反应,A错误;
B.N3-、F-、Al3+核外都有两层电子,S2-有三层电子,S2-半径最大,N3-、F-、Al3+电子层数相同,层同看序数,序小半径大,所以S2->N3->F->Al3+,B错误;
C.H2S有还原性,浓H2SO4有强氧化性,浓硫酸能将H2S氧化成S,C正确;
D.氮氧化物中都是非金属元素,含共价键,Al2O3含离子键,D错误。
答案选C。

练习册系列答案
相关题目