题目内容
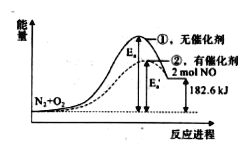
【题目】在其他条件相同时,反应N2+O2=2NO分别在有、无催化剂时的能量变化如下图所示,下列说法中不正确的是( )
A. 该反应中反应物的总能量比生成物的总能量低
B. 0.2 mol NO完全分解成N2和O2时共放出热量18.26 kJ
C. 加入催化剂可以改变反应的活化能
D. 加入催化剂能改变反应的焓变
【答案】D
【解析】
A.从图示可知,反应物的总能量低于生成物的总能量,为吸热反应,故A正确;
B.根据图示可知:反应生成2molNO时,吸收热量为182.6kJ,所以2molNO完全分解成N2和O2时共放出热量182.6kJ,则0.2molNO完全分解成N2和O2时共放出热量18.26kJ,故B正确;
C.由图可知,催化剂能降低反应的活化能,故C正确;
D.加入催化剂,降低反应活化能,但反应的焓变不变,故D错误。
故选D。

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
【题目】有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验装 置 |
|
|
|
|
部分实验现象 | a极质量减小;b极质量增加 | b极有气体产生;c极无变化 | d极溶解;c极有气体产生 | 电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>dB.b>c>d>aC.d>a>b>cD.a>b>d>c