题目内容
【题目】一种以肼(N2H4)为燃料的新型环保电池的工作原理如图所示。下列说法正确的是

A. 电极A的电势比电极B的低
B. 电极A的电极反应式为N2H4-4e-+4OH-===N2+4H2O
C. 电极B发生氧化反应
D. 每消耗11.2L的O2,转移的电子数为2NA
【答案】A
【解析】
根据原电池原理分析解答。
A. 电极A为负极,故A的电势比电极B的低,故A正确;
B. 由图示可知,固体电解质中存在阳离子而不是氢氧根,电极A的电极反应式为:N2H4-4e-+2O2-===N2+2H2O,故B错误;
C. 电极B为正极,氧气得电子生成阳离子,发生还原反应,故C错误;
D. 没有说明是否在标准状况下,所以11.2L的O2,转移的电子数不能确定,故D错误。
故选A。

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
【题目】在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)![]() N2O4g)(无色),如图所示.
N2O4g)(无色),如图所示.
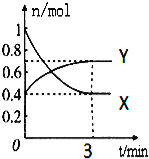
(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线.
(2)若降低温度,则v(正) ,v(逆) .(填“加快”或“减慢”或“不变”).
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3mol/(Ls),乙中v(N2O4)=6mol/(Lmin),则 中反应更快.
(4)在0到3min中内N2O4的反应速率为 .
(5)下列叙述能说明该反应已达到化学平衡状态的是(填标号) ;
A.v(NO2)=2v(N2O4) |
B.容器内压强不再发生变化 |
C.X的体积分数不再发生变化 |
D.容器内气体原子总数不再发生变化 |
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X.