题目内容
【题目】向FeBr2、FeI2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示,下列有关说法中不正确的是( )
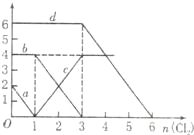
A.d曲线代表溶液中Br﹣变化情况
B.原溶液中FeI2的物质的量为2mol
C.原溶液中n(Fe2+):n(Br﹣)=2:3
D.当通入2mol Cl2时,溶液中离子反应为:2Fe2++2I﹣+2Cl2═2Fe3++I2+4Cl﹣
【答案】B
【解析】
试题分析:首先根据氧化还原反应中:氧化剂的氧化性>氧化产物的氧化性,还原剂的还原性>还原产物的还原性,氧化剂先氧化还原性强的离子,再氧化还原性弱的离子,判断离子的反应先后顺序,然后根据图象判断参加反应的各离子的物质的量,以此解答该题.
解:A.反应2Fe2++Br2=2Fe3++2Br﹣中,还原剂Fe2+的还原性强于还原产物Br﹣,所以还原性:Fe2+>Br﹣,反应2Fe3++2I﹣=2Fe2++I2中,还原剂I﹣的还原性强于还原产物Fe2+,所以还原性:I﹣>Fe2+,所以还原性I﹣>Fe2+>Br﹣,则通入氯气,先与碘离子反应,再与Fe2+反应,a对应氯气与碘离子的反应,c对应氯气与亚铁离子反应,当加3mol氯气时溴离子开始反应,则d曲线代表溶液中Br﹣变化情况,故A正确;
B.通入氯气后,碘离子先被氧化,其次是亚铁离子,最后是溴离子,在通入氯气的量为0~1mol的过程中,碘离子从最大量降到0,即得到碘离子的物质的量为2mol,通入氯气的量为1~3mol的过程中,亚铁离子从4mol降到0,三价铁的量逐渐增大,所以含有亚铁离子共4mol,在通入氯气的量为3~6mol的过程中溴离子从6ml降到0,所以溴离子的物质的量是6mol,即FeBr2的物质的量为3mol,FeI2的物质的量为1mol,故B错误;
C.由B可知,亚铁离子是4mol,溴离子的物质的量是6mol,n(Fe2+):n(Br﹣)=2:3,故C正确;
D.当通入2molCl2时,2mol的I﹣消耗氯气1mol,余下的1mol氯气再与2molFe2+反应,即溶液中发生的离子反应可表示为2Fe2++2I﹣+2Cl2=2Fe3++I2+4Cl﹣,故D正确.
故选B.