题目内容
【题目】下列叙述错误的是
A. 常温下,pH=3的盐酸与pH=11的氨水溶液中水的电离程度相同
B. 常温下两种溶液①0.1mol/L CH3COOH溶液 ②0.3mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积的混合液,c(H+):①>②
C. 室温下向10mL pH=3的醋酸溶液中加入水稀释后溶液中c(CH3COO-)/[c(CH3COOH)·c(OH-)]不变
D. MOH和ROH两种碱的溶液分别加水稀释时,pH变化如图所示则稀释前,c(ROH)<10c(MOH)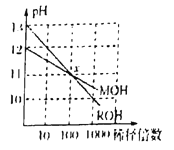
【答案】B
【解析】A、常温下,pH=3的盐酸抑制水电离,水电离的c(H+)=10-11mol·L-1,pH=11的氨水抑制水电离,水电离的c(OH-)=10-11mol·L-1,pH=3的盐酸与pH=11的氨水溶液中水的电离程度相同,故A正确;B、①0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积的混合液成为0.05mol·L-1的CH3COONa,②0.3mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积的混合液中溶质为0.1mol·L-1的CH3COOH和0.05mol·L-1的CH3COONa,醋酸的电离大于水解,所以c(H+):①<②,故B错误;C. 室温下向10mLpH=3的醋酸溶液中加入水稀释后溶液中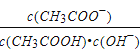 =
=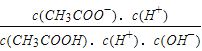 =ka/kw,温度不变,两常数的比值不变。故C正确;D、ROH为强碱,稀释前浓度为0.1mol·L-1,MOH的pH=12时稀释100倍,pH变为11,则说明MOH为弱碱,稀释前MOH的浓度大于0.01mol·L-1,则稀释前c(ROH)<10c(MOH),故D正确;故选B。
=ka/kw,温度不变,两常数的比值不变。故C正确;D、ROH为强碱,稀释前浓度为0.1mol·L-1,MOH的pH=12时稀释100倍,pH变为11,则说明MOH为弱碱,稀释前MOH的浓度大于0.01mol·L-1,则稀释前c(ROH)<10c(MOH),故D正确;故选B。

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目