题目内容
【题目】向恒温恒容密闭容器中充入1 mol X 和1 mol Y,发生反应 X(g)+2Y(g)![]() Z(g)+W(s),下列选项不能说明反应已达平衡状态的是
Z(g)+W(s),下列选项不能说明反应已达平衡状态的是
A.v正(X)=2v逆(Y)B.气体平均密度不再发生变化
C.容器内压强不再变化D.X的浓度不再发生变化
【答案】A
【解析】
A. 在任何时刻都存在:2v正(X)=v正(Y),若v正(X)=2v逆(Y),则v正(Y)= 2v正(X)=4 v逆(Y),说明反应正向进行,未达到平衡状态,A符合题意;
B. 反应混合物中W是固体,若未达到平衡状态,则气体的质量、物质的量都会发生变化,气体的密度也会发生变化,所以当气体平均密度不再发生变化时,说明反应处于平衡状态,B不符合题意;
C. 反应在恒容密闭容器中进行,反应前后气体的物质的量发生变化,所以若容器内压强不再变化,则反应处于平衡状态,C不符合题意;
D. 反应在恒温恒容的密闭容器中进行,若反应未达到平衡状态,则任何气体物质的浓度就会发生变化,所以若X的浓度不再发生变化,说明反应处于平衡状态,D不符合题意;
故合理选项是A。

 53随堂测系列答案
53随堂测系列答案【题目】(1)根据A~E几种烃分子的结构填空。
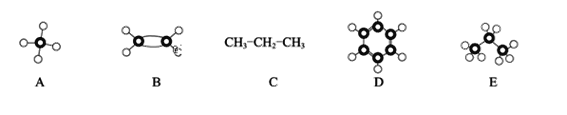
上述分子中属于C的同系物的是_____________(填字母序号)。
(2)随着工业的发展和社会的进步,人们日益关注环境问题。
①下列物质属于室内空气污染物的是__________________(填字母序号,下同);
A CO2 B 甲醛 C N2
②按照垃圾分类的方法,易拉罐瓶属于________________________;
A 可回收物 B 可堆肥垃圾
③工业废水需处理达标后才能排放。下列废水处理的方法合理的是__________。
A 用氯气除去废水中的悬浮物 B 用中和法除去废水中的酸
C 用明矾除去废水中的重金属离子
(3)化学是材料科学发展的基础,合理使用材料有利于人类的生产和生活。
①在一定条件下,将某种单体进行加聚反应得到一种如下图所示的导电性塑料:
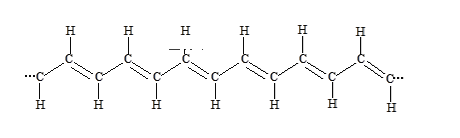
则合成该塑料的单体为___________ (填字母序号,下同);
A 乙炔 B 乙烯 C 乙烷 D 甲烷
②工业炼铁通常采用的方法是__________;
A 加热分解法 B 电解法 C 高温还原法
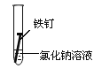
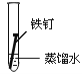
③某同学欲探究铁在NaCl溶液、蒸馏水和空气中锈蚀的快慢,设计了如下实验。
实验序号 | A | B | C |
实验 内容 |
|
|
|
一周后,试管中铁钉锈蚀程度最大的是__________;
④将质量相同的铁片、铜片用导线连接后浸入硫酸铜溶液中,构成原电池,工作一段时间后铜片质量与铁片质量相差12 g,则理论上导线中通过______mol电子。