题目内容
【题目】某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
CH3CH=CH2+CO+H2![]() CH3CH2CH2CHO
CH3CH2CH2CHO![]() CH3CH2CH2OH
CH3CH2CH2OH
其中CO的制备原理:HCOOH![]() CO↑+H2O,并设计出原料气的制备装置(如下图)
CO↑+H2O,并设计出原料气的制备装置(如下图)
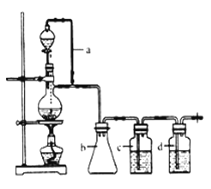
请填写下列空白:
(1)实验室现有锌粒、稀硝酸、稀盐酸、浓硫酸、2-丙醇,从中可以选择合适的试剂制备氢气、丙烯。写出制备丙烯的化学方程式:_______________________。
(2)若用以上装置制备干燥纯净的CO,装置中a的作用是__________,装置中b的作用是_________,c中盛装的试剂是___________。
(3)制丙烯时,还产生少量SO2、CO2及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是___________(填序号)
①饱和Na2SO3溶液 ②酸性KMnO4溶液 ③石灰水 ④无水CuSO4⑤品红溶液
(4)正丁醛经催化加氢得到含少量正丁醛的1-丁醇粗品,为纯化1-丁醇,该小组查阅文献得知:
①R—CHO+NaHSO3(饱和)![]() RCH(OH)SO3Na↓;
RCH(OH)SO3Na↓;
②沸点:乙醚34℃,1-丁醇118℃,并设计出如下提纯路线:

试剂1为______________,操作2为_____________,操作3为_____________。
【答案】(CH3)2CHOH![]() CH2=CHCH3↑+H2O 保证分液漏斗内外压强平衡,便于液体顺利流下 作为安全瓶,防倒吸 NaOH溶液 ④⑤①⑤③② 饱和NaHSO3溶液 萃取 蒸馏
CH2=CHCH3↑+H2O 保证分液漏斗内外压强平衡,便于液体顺利流下 作为安全瓶,防倒吸 NaOH溶液 ④⑤①⑤③② 饱和NaHSO3溶液 萃取 蒸馏
【解析】
根据目标产物及原料的结构特点分析判断由2-丙醇在浓硫酸作用下脱水制备丙烯;根据实验原理及装置特点分析各仪器的作用及所需试剂;根据H2O\二氧化硫、二氧化碳的性质分析检验的方法及顺序;根据提纯路线图中物质的变化分析操作的名称及所用试剂。
(1)根据题干提供的原料分析知,可以用2-丙醇在浓硫酸作用下脱水制备丙烯,反应方程式为:(CH3)2CHOH![]() CH2=CHCH3↑+H2O,故答案为:(CH3)2CHOH
CH2=CHCH3↑+H2O,故答案为:(CH3)2CHOH![]() CH2=CHCH3↑+H2O;
CH2=CHCH3↑+H2O;
(2)根据装置图分析知,导管a可以使得分液漏斗中的压强和烧瓶中压强相等,便于分液漏斗中的液体顺利滴下;制得的CO中含有挥发出的甲酸,可以用NaOH溶液吸收,再用浓硫酸干燥即可得到纯净的CO;装置b可以防止c中液体倒吸进入蒸馏烧瓶,起到安全瓶的作用,故答案为:保证分液漏斗内外压强平衡,便于液体顺利流下;作为安全瓶,防倒吸;NaOH溶液;
(3)首先检验H2O,用无水硫酸铜,若变蓝说明有水,再用品红检验SO2,若品红褪色说明有SO2,用饱和亚硫酸钠溶液可以吸收SO2,再通过酸性高锰酸钾溶液检验SO2是否除尽,最后通入澄清石灰水中,若变浑浊,说明含有CO2,故答案为:④⑤①⑤③②;
(4)由粗品分离出滤液,可见操作1为过滤;则加入试剂1,必须有沉淀生成,故正丁醛中应加入饱和NaHSO3溶液;在滤液中加入乙醚,萃取出1-丁醇,再通过蒸馏将两者分离,所以操作2是萃取,操作3是蒸馏,故答案为:饱和NaHSO3溶液;萃取;蒸馏。