题目内容
3.下表标出的是元素周期表的一部分元素,回答下列问题:
(1)表中用字母标出的14种元素中,化学性质最不活泼的是Ar(用元素符号表示,下同),主族元素中金属性最强的是K,非金属性最强是F,常温下单质为液态的非金属元素是Br;属于过渡元素的是M(该空用字母表示).
(2)B、F、C气态氢化物的化学式分别为H2O、HCl、PH3.
(3)第三周期中原子半径最小的是Cl.
分析 (1)元素周期表中,化学性质最活泼的金属在左下角,化学性质越活泼则金属性越强,非金属性最强的在右上角,溴单质在常温下是液体,M属于过渡元素;
(2)根据元素的化合价确定化学式;
(3)同周期元素原子半径从左到右逐渐减小.
解答 解:根据元素周期表中元素的分布知识,可以知道:A是F,B是O,C是P,D是C,E是Ar,F是Cl,G是S,H是Al,I是Mg,J是Na,K是Ca,L是K,N是Br,M是Tc,M处于d区,属于过渡元素;
(1)元素周期表中,从上到下金属的活泼性逐渐增强,从右到左金属活泼性逐渐增强,所以化学性质最活泼的金属在左下角,应该是K,化学性质越活泼则金属性越强,所以金属性最强的也是K,稀有气体元素化学性质是最稳定的,即Ar化学性质是最稳定,元素周期表中,从下到上元素的非金属性逐渐增强,从左到右非金属性逐渐增强,所以非金属性最强的在右上角,应该是F,溴单质在常温下是液体,属于过渡元素的是M,故答案为:Ar;K;F;Br;M;
(2)根据元素的化合价确定化学式,B、F、C气态氢化物中O、Cl、P的化合价分别为-2、-1、-3,H的化合价为+1,所以它们的化学式分别为H2O、HCl、PH3,故答案为:H2O、HCl、PH3;
(3)同周期元素原子半径从左到右逐渐减小,所以原子半径最小的是Cl,故答案为:Cl.
点评 本题考查了元素周期表和元素周期律的综合应用,熟悉元素在周期表中的位置是解本题关键,注意周期律的灵活运用,难度不大.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
13.氨水显弱碱性的主要原因是( )
| A. | 通常状况下,氨的溶解度不大 | B. | 氨水中的NH3•H2O电离出少量OH- | ||
| C. | 溶于水的氨分子只有少量电离 | D. | 氨本身的弱碱性 |
14.化合物丙由如下反应得到: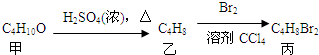 ,丙的结构简式不可能是( )
,丙的结构简式不可能是( )
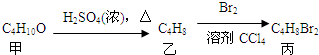 ,丙的结构简式不可能是( )
,丙的结构简式不可能是( )| A. | CH3CH2CHBrCH2Br | B. | CH3CH(CH2Br)2 | C. | CH3CHBrCHBrCH3 | D. | (CH3)2CBrCH2Br |
11.下列反应中,不属于取代反应的是( )
| A. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯 | |
| B. | 在一定条件下苯与氢气反应制环己烷 | |
| C. | 苯与浓硫酸共热制取苯磺酸 | |
| D. | 催化剂存在下,苯与溴反应制溴苯 |
18.用下列一种试剂就可鉴别出甲酸、乙酸、甲酸乙酯和乙酸甲酯,该试剂是( )
| A. | 银氨溶液 | B. | 新制Cu(OH)2悬浊液 | C. | KMnO4(H+)溶液 | D. | NaOH溶液 |
8.下列一卤代烷不能发生消去反应的是( )
| A. | CH3CH2Cl | B. | (CH3)3CCH2Cl | C. | (CH3)3CCl | D. | (CH3)2CHCl |
15.A+、B+、C-、D-四种离子两两组成四种可溶性盐,其中:AC和BD盐溶液pH=7,BC盐溶液pH>7,则下列说法不正确的是( )
| A. | AD盐溶液pH>7 | B. | 在AC盐溶液中c(A+)+c(AOH)=c(C-)+c(HC) | ||
| C. | 酸的电离程度一定是:HD>HC | D. | 碱的电离程度一定是:AOH>BOH |
12.下列排列顺序正确的是( )
| A. | 热稳定性:H2O>H2S>SiH4 | B. | 原子半径:Na>N>Al | ||
| C. | 酸性:H3PO4>H2SO4>HClO4 | D. | 碱性:NaOH>Be(OH)2>Mg(OH)2 |
13.三氯化氮分子中每个原子其最外层均达到8电子稳定结构,且氮与氯的共用电子对偏向于氮原子.下列说法正确的是( )
| A. | 在NCl3分子中N为+3价,跟水发生水解反应的产物是HNO2和HCl | |
| B. | NCl3跟水发生复分解反应的初级产物是NH3和HClO | |
| C. | NCl3发生水解反应生成NH4Cl、O2和Cl2 | |
| D. | NCl3的电子式应表示为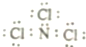 |