题目内容
氯气是重要的化工原料。
(1)氯气溶于水得到氯水,氯水中存在下列反应:Cl2 + H2O H++Cl-+ HClO,其平衡常数表达式为K= 。
H++Cl-+ HClO,其平衡常数表达式为K= 。
(2)工业上常用熟石灰和氯气反应制取漂白粉,化学反应方程式是 。流程如下图所示,其主要设备是氯化塔,塔从上到下分四层。


将含有3%~6%水分的熟石灰从塔顶喷洒而入,氯气从塔的最底层通入。这样加料的目的是 ,处理从氯化塔中逸出气体的方法是 。
(3)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是 ,其原因可能是 ,由此可知(2)中氯化塔设计为四层是为了减少生产中类似副反应的发生。
(1)氯气溶于水得到氯水,氯水中存在下列反应:Cl2 + H2O
 H++Cl-+ HClO,其平衡常数表达式为K= 。
H++Cl-+ HClO,其平衡常数表达式为K= 。(2)工业上常用熟石灰和氯气反应制取漂白粉,化学反应方程式是 。流程如下图所示,其主要设备是氯化塔,塔从上到下分四层。


将含有3%~6%水分的熟石灰从塔顶喷洒而入,氯气从塔的最底层通入。这样加料的目的是 ,处理从氯化塔中逸出气体的方法是 。
(3)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是 ,其原因可能是 ,由此可知(2)中氯化塔设计为四层是为了减少生产中类似副反应的发生。
(1)[c(H+)·c(Cl-)·c(HClO)]/c(Cl2)
(2)2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O
充分接触(或充分吸收);用碱液吸收(或石灰乳或碱石灰或氢氧化钠溶液等)
(3)6OH-+3Cl2=5Cl-+ ClO3-+3H2O 反应放热使温度升高所致
(2)2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O
充分接触(或充分吸收);用碱液吸收(或石灰乳或碱石灰或氢氧化钠溶液等)
(3)6OH-+3Cl2=5Cl-+ ClO3-+3H2O 反应放热使温度升高所致
(1)K=[c(H+)·c(Cl-)·c(HClO)]/c(Cl2)
(2)熟石灰从塔顶喷洒从上向下,氯气从塔的最底层通入从下向上,氯气和熟石灰充分接触、混合,使其反应充分进行;氯气与碱反应,所以用碱液吸收;
(3)氯化塔设计为四层是为了增大散热面积,防止反应过程产生的热量使体系温度升高,副反应增多。
(2)熟石灰从塔顶喷洒从上向下,氯气从塔的最底层通入从下向上,氯气和熟石灰充分接触、混合,使其反应充分进行;氯气与碱反应,所以用碱液吸收;
(3)氯化塔设计为四层是为了增大散热面积,防止反应过程产生的热量使体系温度升高,副反应增多。

练习册系列答案
相关题目
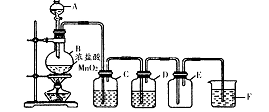
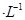 的溶液缓缓通入100 mLCl2(标准状况),溶液由浅绿色逐渐变黄色;继续通人Cl2,溶液黄色加深,变为棕黄色。
的溶液缓缓通入100 mLCl2(标准状况),溶液由浅绿色逐渐变黄色;继续通人Cl2,溶液黄色加深,变为棕黄色。