题目内容
下列属于物理变化的是
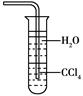
| A.氯气溶于水 | B.食物变质 | C.用四氯化碳萃取碘水中的碘 | D.光合作用 |
C
试题分析:化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断。A、氯气溶于水,与水反应生成氯化氢和次氯酸,属于化学变化.故选项错误;B、食物变质的过程中有对人体有害的新物质生成,属于化学变化,故选项错误;C、萃取过程中没有新物质生成,属于物理变化.故选项正确;D、光合作用中有新物质生成,属于化学变化,故选项错误;故选C。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 H++Cl-+ HClO,其平衡常数表达式为K= 。
H++Cl-+ HClO,其平衡常数表达式为K= 。