题目内容
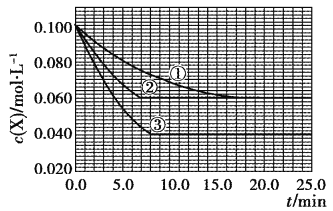
【题目】在密闭容器中,反应X(g)+2Y(g)![]() Z(g)分别在三种不同实验条件下进行,它们的起始浓度均为c(X)=0.100mol·L-1,c(Y)=0.200mol·L-1,c(Z)=0mol·L-1。反应物X的浓度随时间的变化如图所示。下列说法正确的是
Z(g)分别在三种不同实验条件下进行,它们的起始浓度均为c(X)=0.100mol·L-1,c(Y)=0.200mol·L-1,c(Z)=0mol·L-1。反应物X的浓度随时间的变化如图所示。下列说法正确的是
A. 实验②的温度高于实验①的温度
B. 实验②平衡时Y的转化率为60%
C. 实验③与实验①相比,实验③使用了催化剂
D. 反应X(g)+2Y(g)![]() Z(g)的△H>0
Z(g)的△H>0
【答案】D
【解析】
与①比较,②反应速率增大,但与①处于同一平衡状态,则②应为加入催化剂;与①比较,③反应速率增大,可能是升高温度或增大压强,但如是增大压强,减小容器的体积虽然平衡向正反应方向移动,但X的平衡浓度反而增大,不符合图象,则应为升高温度,据此分析解答。
A. 因为①、②的起始浓度相同、平衡浓度相同,②的反应速率比①快,所以实验②应是在有催化剂的条件下进行的,实验②的温度与实验①的温度相同,故A错误;
B. 从图中可以看出,实验②平衡时X的浓度变化量为0.04mol/L,则Y的浓度变化量为0.08mol/L,Y的转化率为40%,故B错误;
C. 实验③与实验①相比,X的浓度变化量大,说明平衡正向移动,而使用催化剂平衡不移动,故C错误;
D. 实验③与实验①相比,X的浓度变化量大,说明平衡正向移动,且化学反应速率加快,故此时的反应条件只能为升温,由此可见,正反应是吸热反应,△H>0,故D正确。
故答案选D。

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案【题目】下列根据实验事实得出的结论错误的是( )
实验事实 | 结论 | |
A. | 某溶液中加入BaCl2溶液有白色沉淀生成 | 该溶液中一定含有SO42- |
B. | 加热时,铜能与浓硫酸反应 | 浓硫酸有强氧化性 |
C. | 某分散系具有丁达尔效应 | 该分散系是胶体 |
D. | Al(OH)3既能与盐酸反应,也能与NaOH溶液反应 | Al(OH)3是两性氢氧化物 |
A.AB.BC.CD.D