题目内容
16.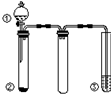 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
利用如图所示装置进行下列实验,能得出相应实验结论的是( )| 选项 | ① | ② | ③ | 实验结论 |
| A | 稀硫酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:S>C>Si |
| B | 稀硝酸 | Na2S | AgNO3与AgCl的浊液 | Ksp(AgCl)>Ksp(Ag2S) |
| C | 浓盐酸 | MnO2 | NaOH溶液 | 氧化性:MnO2>Cl2 |
| D | 浓硫酸 | 蔗糖 | 酸性KMnO4溶液 | 浓硫酸具有酸性、脱水性 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.发生强酸制取弱酸的反应,利用最高价含氧酸的酸性可比较非金属性;
B.硝酸与硫化钠发生氧化还原反应;
C.浓盐酸与二氧化锰反应需要加热;
D.浓硫酸使蔗糖碳化后,C与浓硫酸发生氧化还原反应生成二氧化硫,二氧化硫与高锰酸钾发生氧化还原反应.
解答 解:A.发生强酸制取弱酸的反应,可知酸性为硫酸>碳酸>硅酸,则非金属性为S>C>Si,故A正确;
B.硝酸与硫化钠发生氧化还原反应,不能生成硫化氢气体,则不能实现AgCl沉淀转化为Ag2S沉淀,则不能比较二者的Ksp,故B错误;
C.浓盐酸与二氧化锰反应需要加热,图中没有加热装置,则不能比较MnO2、Cl2的氧化性,故C错误;
D.浓硫酸使蔗糖碳化后,C与浓硫酸发生氧化还原反应生成二氧化硫,二氧化硫与高锰酸钾发生氧化还原反应,则浓硫酸具有强氧化性、脱水性,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,涉及酸性比较、氧化还原反应、沉淀生成与转化、物质的制备及性质等,把握物质的性质、反应原理为解答的关键,侧重分析与实验能力的考查,注意实验装置的作用及评价性分析,题目难度不大.

练习册系列答案
相关题目
7.下列物质性质与应用对应关系正确的是( )
| A. | 氯化镁属于电解质,工业上可用电解其溶液的方法制镁 | |
| B. | 钠钾合金的硬度小,可用作快中子反应堆的热交换剂 | |
| C. | Fe2O3是红棕色固体,可以制成红色的油漆、涂料 | |
| D. | 溴单质在CCl4中的溶解度大,可用CCl4萃取Br- |
4.下列事实、离子方程式及其对应关系均正确的是( )
| A. | 向Ag2S浊液中滴加少量稀NaCl溶液,黑色沉淀逐渐变成白色:Ag2S+Cl-?AgCl+S2- | |
| B. | 向K2Cr2O7溶液中滴加少量浓H2SO4,溶液变为黄色:Cr2O72-(橙色)+H2O?2CrO42-(黄色)+2H+ | |
| C. | 向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后溶液变蓝:4H++4I-+O2=2I2+2H2O | |
| D. | 向水杨酸(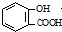 )中滴加NaHCO3溶液,放出无色气体: )中滴加NaHCO3溶液,放出无色气体: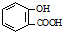 +2HCO3-→ +2HCO3-→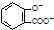 +2CO2↑+2H2O +2CO2↑+2H2O |
11.各可逆反应达平衡后,改变反应条件,其变化趋势正确的是( )
| A. | 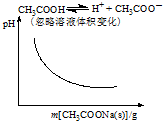 | B. | 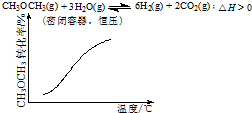 | ||
| C. |  | D. | 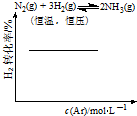 |
8.实验室制取氯气并回收氯化锰,能达到该实验目的装置是( )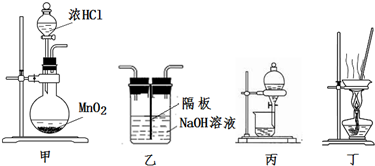

| A. | 用装置甲制取氯气 | |
| B. | 用装置丙分离二氧化锰和氯化锰溶液 | |
| C. | 用装置乙吸收制取氯气的尾气 | |
| D. | 用装置丁蒸干氯化锰溶液制 MnCl2•4H2O |
6.设nA为阿伏加德罗常数的数值.下列说法正确的是( )
| A. | 常温常压下,1mol21H2含有nA个质子 | |
| B. | 1molCu与足量FeCl3溶液充分反应转移了2nA个电子 | |
| C. | 含49gH2SO4的硫酸溶液中含有nA个氢原子 | |
| D. | 标准状况下,22.4L甲醇含有nA个分子 |
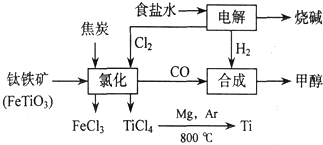
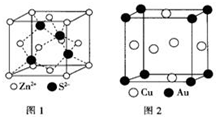 1967年舒尔滋提出金属互化物的概念,其定义为固相金属间化合物拥有两种或两种以上的金属元素,如Cu9Al4、Cu5Zn8 等.回答下列问题:
1967年舒尔滋提出金属互化物的概念,其定义为固相金属间化合物拥有两种或两种以上的金属元素,如Cu9Al4、Cu5Zn8 等.回答下列问题: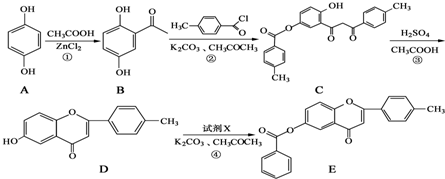
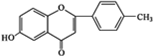 +
+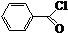 $\stackrel{K_{2}CO_{3}、CH_{3}COCH_{3}}{→}$
$\stackrel{K_{2}CO_{3}、CH_{3}COCH_{3}}{→}$ +HCl.
+HCl.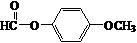 .
.