题目内容
【题目】某铝合金中含有元素:铝、镁、铜、碳,为测定该合金中铝的含量。
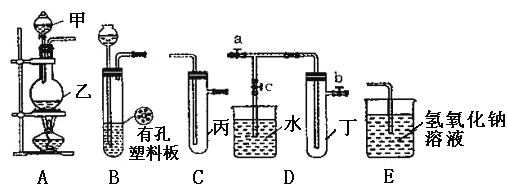
Ⅰ 甲同学设计如下实验:
(1)称取样品a g(精确到0.1 g),溶于足量稀盐酸,过滤。
(2)向步骤(1)所得滤液中加入过量的氢氧化钠溶液,过滤并洗涤滤渣。有关反应的离子方程式是_________________________________、____________________________________________。
(3)向步骤(2)所得滤液中通入过量的二氧化碳气体,过滤并洗涤滤渣。有关反应的离子方程式是_________________________________、____________________________________________。
(4)将步骤(3)所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为b g。有关反应的化学方程式是_________________________________。原样品中铝的质量分数是__________。
Ⅱ 乙同学认为也可以向一定质量的样品中直接加足量氢氧化钠溶液充分反应后,将剩余固体过滤、洗涤、干燥后称量,即可计算该合金中铝的含量。有关反应的离子方程式是____________________________________________。
【答案】Mg2++2OH-===Mg(OH)2↓ Al3++4OH-===AlO2-+2H2O OH-+CO2===HCO3- AlO2-+CO2+2H2O===Al(OH)3↓+HCO3- 2Al(OH)3=△=Al2O3+3H2O 900b/17a% 2Al+2OH-+2H2O ===2AlO2-+3H2↑
【解析】
Ⅰ(2)将合金溶于足量稀盐酸,反应生成氯化镁和氯化铝,再加入过量氢氧化钠溶液,氯化镁与氢氧化钠反应生成氢氧化镁和氯化钠,反应的离子方程式为Mg2++2OH-=Mg(OH)2↓;氯化铝与足量的氢氧化钠反应生成偏铝酸钠、氯化钠和水,反应的离子方程式为Al3++4OH-=AlO2-+2H2O;
(3)向步骤(2)所得滤液中通入过量的二氧化碳气体,二氧化碳与氢氧化钠反应生成碳酸氢钠,反应的离子方程式为OH-+CO2=HCO3-;二氧化碳与偏铝酸钠反应生成氢氧化铝沉淀和碳酸氢钠,反应的离子方程式是AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(4)将步骤(3)所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为b g。有关反应的化学方程式是2Al(OH)3![]() Al2O3+3H2O;
Al2O3+3H2O;
所得b g固体为Al2O3,故合金中含Al的质量分数为![]() ×100%=
×100%=![]() %;
%;
Ⅱ 乙同学认为也可以向一定质量的样品中直接加足量氢氧化钠溶液充分反应后,将剩余固体过滤、洗涤、干燥后称量,铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的离子方程式是2Al+2OH-+2H2O =2AlO2-+3H2↑。

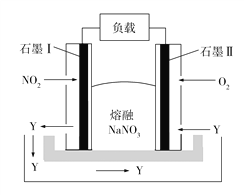
【题目】用如图装置研究电化学原理,下列分析中错误的是

选项 | 连接 | 电极材料 | 分析 | |
a | b | |||
A | K1K2 | 石墨 | 铁 | 模拟铁的吸氧腐蚀 |
B | K1K2 | 锌 | 铁 | 模拟钢铁防护中牺牲阳极的阴极保护法 |
C | K1K3 | 石墨 | 铁 | 模拟电解饱和食盐水 |
D | K1K3 | 铁 | 石墨 | 模拟钢铁防护中外加电流的阴极保护法 |
A. A B. B C. C D. D