题目内容
【题目】海洋是一个巨大的化学资源宝库,下面是海水资源综合利用的部分流程图。

(1)步骤①中除去粗盐中杂质(Mg2+、SO![]() 、Ca2+),加入的药品顺序正确的是__________。
、Ca2+),加入的药品顺序正确的是__________。
A. NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B. BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸
C. NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸
D. BaCl2溶液→Na2CO3溶液→NaOH溶液→过滤后加盐酸
(2)步骤⑤中已获得Br2,步骤⑥中又用SO2的水溶液将Br2吸收,其目的是___________。
(3)写出步骤⑥中发生反应的离子方程式:_______________。
(4)把溴吹入到SO2的水溶液的气体X最可能用下面的___(填序号)。
A. 乙烯 B. 空气 C. 氩气 D. CO2
(5)由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由弱到强的顺序是___________。
(6)钛是航空、军工、电力等方面的必需原料。常温下钛不与非金属、强酸反应,红热时,却可与常见的非金属单质反应。目前大规模生产钛的方法是:TiO2、炭粉混合,在高温条件下通入Cl2制得TiCl4和一种可燃性气体。该反应的化学方程式为______。
【答案】BCD 提高溴的富集程度 Br2+SO2+2H2O=4H++2Br-+SO4 2 - B Cl-<Br-<SO2 TiO2+2C+2Cl2![]() TiCl4+2CO
TiCl4+2CO
【解析】
海水分离得到粗盐、淡水和母液卤水,粗盐提纯得到精盐,母液中加入氢氧化钙沉淀镁离子生成氢氧化镁沉淀,过滤得到沉淀在盐酸中溶解得到氯化镁溶液,浓缩结晶、得到氯化镁晶体,氯化氢气流中脱水得到氯化镁,电解熔融氯化镁得到金属镁和氯气;得到的NaBr溶液中通入氯气氧化溴离子生成溴单质,用热空气吹出溴单质和二氧化硫发生氧化还原反应生成硫酸和溴化氢,吸收液中通入氯气氧化溴离子生成单质溴,蒸馏冷却分离得到纯溴,据此分析解答。
(1)除去粗盐中的Ca2+、Mg2+、SO42-,通过加氯化钡除SO42-离子,加碳酸钠除Ca2+离子,加NaOH除去Mg2+离子,同时碳酸钠可以除去过量的钡离子,过滤后,加入盐酸调节pH除去过量的碳酸根离子和氢氧根离子,据此分析解答;
(5)根据氧化还原反应中还原剂的还原性大于还原产物分析判断;
(6) TiO2、炭粉混合在高温下通入氯气制得TiCl4和一种可燃性气体,根据质量守恒定律,该气体为一氧化碳,据此分析解答。
(1) 除去粗盐中杂质(Mg2+、SO42-、Ca2+),通过加氯化钡除SO42-离子,然后再加碳酸钠除Ca2+离子,同时碳酸钠可以除去过量的钡离子,如果加反了,过量的钡离子就没法除去,加NaOH除去Mg2+离子顺序不受限制,因为过量的氢氧化钠加盐酸就可以调节了,将三种离子除完,过滤后加盐酸除去过量的氢氧根离子和碳酸根离子;A.NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸,加入的氯化钡溶液中钡离子不能除去,故A错误;B.BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸,符合除杂和提纯的要求,故B正确;C.NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸,符合除杂和提纯的要求,故C正确;D.BaCl2溶液→Na2CO3溶液→NaOH溶液→过滤后加盐酸,符合除杂和提纯的要求,故正确;故答案为:BCD;
(2)步骤⑤中已获得Br2,低浓度的Br2溶液在提取时消耗过多的原料和能源,步骤⑥中又将Br2还原为Br-,目的是转化为HBr后易被氧化剂氯气氧化为溴单质,用于富集溴元素,故答案为:提高溴的富集程度;
(3)步骤⑥中二氧化硫与溴单质发生氧化还原反应,反应的化学方程式为:Br2+SO2+2H2O═H2SO4+2HBr,离子方程式为Br2+SO2+2H2O=4H++2Br-+SO42-,故答案为:Br2+SO2+2H2O=4H++2Br-+SO42-;
(4)把溴吹出的气体X,廉价且不和溴反应,吹出的溴单质用碳酸钠溶液吸收,二氧化碳能够与碳酸钠溶液反应,乙烯和溴发生加成反应,氩气生产成本高,所以工业上最适宜选用空气,故答案为:B;
(5)苦卤中通入Cl2置换出Br2,吹出后用SO2吸收转化为Br-,反复多次,以达到富集溴的目的。由海水提溴过程中的反应中还原剂的还原性大于还原产物,2Br-+Cl2=Br2+2Cl-;反应中还原剂Br-的还原性大于还原产物Cl-;Br2+SO2+2H2O=H2SO4+2HBr,反应中还原剂SO2的还原性大于还原产物Br-;可得出Cl-、SO2、Br-还原性由弱到强的顺序是Cl-<Br-<SO2,故答案为:Cl-<Br-<SO2;
(6) TiO2、炭粉混合在高温下通入氯气制得TiCl4和一氧化碳,该反应的化学方程式为:TiO2+2C+2Cl2 ![]() TiCl4+2CO,故答案为:TiO2+2C+2Cl2
TiCl4+2CO,故答案为:TiO2+2C+2Cl2 ![]() TiCl4+2CO。
TiCl4+2CO。

 阅读快车系列答案
阅读快车系列答案【题目】标号为①~⑩的元素,在元素周期表中的位置如下:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① | ② | ||||||
2 | ③ | ④ | ⑤ | ⑥ | ||||
3 | ⑦ | ⑧ | ⑨ | ⑩ |
试回答下列问题:
(1)写出元素③的名称__。
(2)①和④号元素形成的化合物的化学式为__,用电子式表示其形成过程为__。
(3)⑦和⑧号元素的最高价氧化物的水化物的碱性是:__﹥__
(4)①、⑤、⑦号元素形成的一种化合物的电子式是__,在该化合物中既含有__键,又含有__键。
【题目】唐山市打造“山水园林城市”,因此研究NOx、SO2等大气污染物的妥善处理具有重要意义。
(1)SO2的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的SO2。已知吸收过程中相关反应的热化学方程式如下:
SO2(g)+NH3·H2O(aq)![]() NH4HSO3(aq) ΔH1=a kJ·mol1;
NH4HSO3(aq) ΔH1=a kJ·mol1;
NH3·H2O(aq)+ NH4HSO3(aq)![]() (NH4)2SO3(ag)+H2O(l) ΔH 2=b kJ·mol1;
(NH4)2SO3(ag)+H2O(l) ΔH 2=b kJ·mol1;
2(NH4)2SO3(aq)+O2(g)![]() 2(NH4)2SO4(aq) ΔH 3=c kJ·mol1。
2(NH4)2SO4(aq) ΔH 3=c kJ·mol1。
则反应2SO2(g)+4NH3·H2O(aq)+O2(g) ![]() 2(NH4)2SO4(aq)+2H2O(l)的ΔH =____kJ·mol1。
2(NH4)2SO4(aq)+2H2O(l)的ΔH =____kJ·mol1。
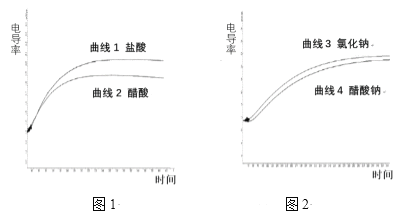
(2)以乙烯(C2H4)作为还原剂脱硝(NO),脱硝机理如图1,则总反应的化学方程式为_______;脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2,为达到最佳脱硝效果,应采用的条件是______。

(3)T1温度时在容积为2L的恒容密闭容器中发生反应:2NO(g)+O2(g)![]() 2NO2(g) △H<0。实验测得:υ正=υ(NO)消耗=2υ(O2)消耗=k正c2(NO)·c(O2),υ逆=(NO2) 消耗=k逆c2(NO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(NO)、n(O2)如表:
2NO2(g) △H<0。实验测得:υ正=υ(NO)消耗=2υ(O2)消耗=k正c2(NO)·c(O2),υ逆=(NO2) 消耗=k逆c2(NO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(NO)、n(O2)如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 1 | 0.6 | 0.4 | 0.2 | 0.2 | 0.2 |
n(O2)/mol | 0.6 | 0.4 | 0.3 | 0.2 | 0.2 | 0.2 |
①T1温度时k正/k逆=__________ L/mol。
②若将容器的温度改变为T2时其k正=k逆,则T2__________T1(填“>”、“<”或“=")。
(4)已知:N2(g)+O2(g)![]() 2NO(g) △H=+181.5 kJ·mol-1,某科研小组尝试利用固体表面催化工艺进行NO的分解。若用
2NO(g) △H=+181.5 kJ·mol-1,某科研小组尝试利用固体表面催化工艺进行NO的分解。若用![]() 、
、![]() 、
、![]() 和
和![]() 分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如图所示。从吸附到解吸的过程中,能量状态最低的是___(填字母序号)。
分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如图所示。从吸附到解吸的过程中,能量状态最低的是___(填字母序号)。

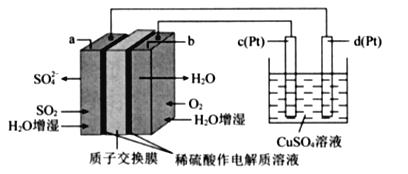
(5)利用电解法处理高温空气中稀薄的NO(O2浓度约为NO浓度的10倍),装置示意图如下,固体电解质可传导O2-

①阴极的电极反应式为______。
②消除一定量的NO所消耗的电量远远大于理论计算量,可能的原因是(不考虑物理因素)_________。
【题目】将气体X通入溶液A(如下图,尾气吸收装置略)中,实验现象能够支持结论的是

选项 | 气体X | 溶液A及反应现象 | 结论 |
A. | 乙醇与浓硫酸共热170℃产生的气体 | Br2的水溶液由橙黄色变为无色 | 乙烯与溴发生反应 |
B. | 电石与饱和食盐水反应产生的气体 | KMnO4酸性溶液紫色逐渐变浅 | 乙炔被高锰酸钾酸性溶液氧化 |
C. | 溴乙烷与氢氧化钠醇溶液共热生成的气体 | Br2的水溶液由橙黄色变为无色 | 乙烯与溴发生反应 |
D. | 碳酸钠固体与醋酸溶液反应产生的气体 | 苯酚钠溶液中出现白色沉淀 | 碳酸的酸性强于苯酚 |
A. A B. B C. C D. D